题目内容
2.新华网达卡2010年8月6日电,为了解决生活用水问题,孟加拉政府在国际援助机构帮助下在全国各地打了数百万口深层管井,后来使用这些深层管井的居民逐渐开始出现砷中毒症状.经专家调查发现,孟加拉国土壤深层自然形成的砷含量非常高,目前数千万民众受到砷污染威胁.下列有关说法正确的是( )| A. | 砷(As)位于周期表第4周期第ⅤA族 | B. | 气态氢化物稳定性:AsH3>PH3>NH3 | ||
| C. | 含氧酸酸性:H3AsO4>HNO3>H3PO4 | D. | 氢化物沸点:AsH3>PH3>NH3 |
分析 A、砷有四个电子层,最个层有5个电子;
B、非金属性越强气态氢化物越稳定;
C、非金属性越强最高价氧化物对应水化物的酸必越强;
D、氨分子间存在氢键.
解答 解:A、砷有四个电子层,最个层有5个电子,所以位于周期表第4周期第ⅤA族,故A正确;
B、非金属性:As<P<N,所以气态氢化物稳定性:AsH3<PH3<NH3,故B错误;
C、非金属性:As<P<N,所以酸性:HNO3>H3PO4>H3AsO4,故C错误;
D、氨分子间存在氢键,所以氢化物沸点:NH3>AsH3>PH3,故D错误;
故选A.
点评 本题考查元素的非金属性的递变规律,氢化物的稳定性和酸性的比较,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.把9.2g Na和4.2g Si同时投入适量水中,在标况下产生氢气的体积是( )
| A. | 2.8L | B. | 5.6L | C. | 11.2L | D. | 22.4L |
10.据报道,碳纳米管是碳原子形成的大分子,其导电性是铜的1万倍;N5可以做烈性炸药.下列叙述正确的是( )
| A. | 金刚石和纳米管互为同分异构体 | B. | N5和N2互为同素异形体 | ||
| C. | 14C的质子数为14 | D. | C原子半径比N原子半径小 |
17.下列物质一定属于同系物的是( )


| A. | ⑤和⑦ | B. | ③和④? | C. | ①、②和③? | D. | ④、⑥和⑧ |
7.在一密闭容器中,反应aA(g)?bB(g)达平衡后,保持温度不变,将容器体积压缩至一半,当达到新的平衡时,B的浓度是原来的160%,则( )
| A. | a>b | B. | 物质A的转化率增大了 | ||
| C. | 物质A的质量分数减小了 | D. | 平衡向逆反应方向移动了 |
12.下列各离子组中,在溶液中能够大量共存的一组是( )
| A. | AlO2-、SO42-、Cl-、K+ | B. | Al3+、Ca2+、HCO3-、Na+ | ||
| C. | Fe3+、NH4+、SO42-、SCN- | D. | H+、Cl-、Na+、HS- |
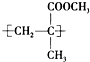 .
. ;
;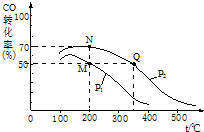 减少污染、保护环境是全世界最热门的课题.
减少污染、保护环境是全世界最热门的课题.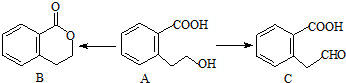
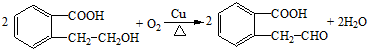 .
.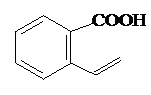 或
或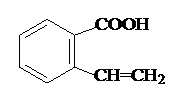 .
.