题目内容
【题目】甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
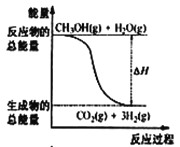
①CH3OH(g)+H2O(g) = CO2(g)+3H2(g) △H=+49. 0 kJ·mol-1
②CH3OH(g)+![]() O2(g) = CO2(g)+2H2(g) △H=-192. 9 kJ·mol-1
O2(g) = CO2(g)+2H2(g) △H=-192. 9 kJ·mol-1
下列说法正确的是
A.CH3OH的燃烧热为192. 9 kJ·mol-1
B.根据②推知反应:CH3OH(l) +![]() O2(g) =CO2(g) +2H2(g) △H >-192. 9kJ·mol-1
O2(g) =CO2(g) +2H2(g) △H >-192. 9kJ·mol-1
C.CH3OH转变成H2的过程一定要吸收能量
D.反应①中的能量变化如图所示
【答案】B
【解析】
A.燃烧热是1mol可燃物完全燃烧产生稳定的氧化物时放出的热量,H2不是氧化物,属于单质,H2燃烧放出热量,因此CH3OH的燃烧热大于192. 9 kJ·mol-1,A错误;
B.等质量的液体物质含有的能量比气态的低,反应物含有的能量越低,反应放出的热量就越少,该反应的反应热就越大,所以根据②推知反应:CH3OH(l) +![]() O2(g) =CO2(g) +2H2(g) △H >-192. 9kJ·mol-1,B正确;
O2(g) =CO2(g) +2H2(g) △H >-192. 9kJ·mol-1,B正确;
C.根据已知的两个热化学方程式可知:CH3OH转变成H2的过程可能要吸收能量,也可能要放出能量,C错误;
D.反应①是吸热反应,反应物的能量比生成物的能量低,所以不能用图中的能量变化表示,D错误;
答案选B。

练习册系列答案
相关题目