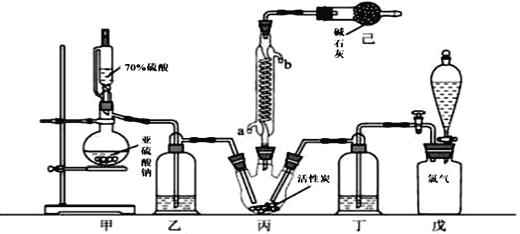
��Ŀ����
����Ŀ��������̼�IJ����������������ҹ���Դ�����һ����Ҫս�Է���չ��һ����Ҫ�����˲�ҵ��
��1����֪��CH4��CO��H2��ȼ���ȷֱ�Ϊ890kJmol��1��283kJmol��1��285.8kJmol��1���������з�Ӧ�ķ�Ӧ�ȡ�CO2��g��+CH4��g����2CO��g��+ 2H2��g����H��___________kJmol��1��
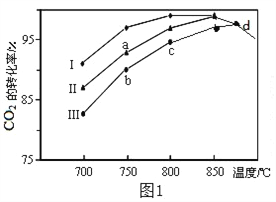
��2�����÷����е�CO2Ϊԭ����ȡ�״�����Ӧ����ʽΪ��CO2��3H2![]() CH3OH��H2O����������ͬ���ü״��ϳɷ�Ӧ�ڲ�ͬ�������������·�Ӧ��ͬʱ���CO2��ת�����淴Ӧ�¶ȵı仯��ͼ����ʾ��
CH3OH��H2O����������ͬ���ü״��ϳɷ�Ӧ�ڲ�ͬ�������������·�Ӧ��ͬʱ���CO2��ת�����淴Ӧ�¶ȵı仯��ͼ����ʾ��
�ٸ÷�Ӧ�Ħ�H_____0�������������
��d�㲻ͬ��������������CO2��ת������ͬ��ԭ����________��
 ��
�� 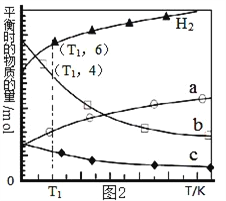
��3���ö�����̼���������ϳɵ�̼ϩ������ʼʱ��0.1MPa��n��H2����n��CO2��=3��1��Ͷ�ϱȳ��뷴Ӧ���У�������Ӧ��2CO2��g��+6H2��g��![]() C2H4��g��+4H2O��g����H����ͬ�¶���ƽ��ʱ��������̬���ʵ����ʵ�����ͼ2��ʾ��
C2H4��g��+4H2O��g����H����ͬ�¶���ƽ��ʱ��������̬���ʵ����ʵ�����ͼ2��ʾ��
�ٸ÷�Ӧ��_________�Է����У�����¡����¡�����
��b������������______________��
��T1�¶��µ�ƽ��ת����Ϊ_________________���������ʼ״̬��ƽ��ʱ�����ƽ������������İٷ���Ϊ______________��������λ��Ч���֣���
���𰸡� +247.6 �� ���ﵽƽ��״̬��������Ӱ��ƽ��ת���� ���� H2O 50% 23.1%
����������1������CH4��H2����CO��ȼ���ȷֱ�д��ȼ�յ��Ȼ�ѧ����ʽ��
��O2��g��+2H2��g��=2H2O��l����H=-571.6kJmol -1��
��CH4��g��+2O2��g��=CO2��g��+2H2O��l����H=-890kJmol-1��
��2CO��g��+O2��g��=2CO2��g����H=-566 kJmol-1��
���ø�˹���ɽ���-��-�ۿɵã� CO2��g��+CH4��g����2CO��g��+ 2H2��g����H��+247.6 kJmol��1��
��2����ͼ����֪���ü״��ϳɷ�Ӧ�ڲ�ͬ���������������������·�Ӧ��ͬʱ���CO2��ת�������ŷ�Ӧ�¶ȵ�������������С��˵������Ӧ�ﵽƽ��״̬�������¶Ȼ�ѧƽ�����淴Ӧ�����ƶ������Ը÷�ӦΪ���ȷ�Ӧ���ٸ÷�Ӧ����H ��0.��d�㲻ͬ����������������������CO2��ת������ͬ��ԭ�����ڴ��¶��¸÷�Ӧ���ﵽƽ��״̬��������Ӱ��ƽ��ת���ʡ�
��3����ͼ2��֪����Ӧ����������ƽ�������¶����߶����������Ը÷�ӦΪ���ȷ�Ӧ���������ߵı仯���ƣ������жϳ�a��b��c�������߷ֱ��ʾ������̼��ˮ����ϩ���ٸ÷�Ӧ��H<0����S<0��ֻ���ڵ����²��ܱ�֤��H-T��S<0�����Ը÷�Ӧ�ڵ����Է����С����ۺϷ�Ӧ�и���ֵĻ�ѧ�����������ߵı仯���ƽ��з����������жϳ�b������������H2O������ʼʱ��0.1MPa��n��H2����n��CO2��=3��1��Ͷ�ϱȳ��뷴Ӧ���У�������Ӧ��2CO2��g��+6H2��g��![]() C2H4��g��+4H2O��g����Ͷ�ϱ��뻯ѧ������֮����ͬ���������ַ�Ӧ���ƽ��ת��������ͬ�ġ���ͼ2��֪��T1�¶��£�������ˮ��ƽ�����ֱ�Ϊ6mol��4mol��˵�������ı仯��Ҳ��6mol�����Ը÷�Ӧ��ƽ��ת����Ϊ50%.����ʼ״̬�������Ͷ�����̼�����ʵ����ֱ�Ϊ12mol��4mol����Ӧ���ƽ����Է�������Ϊ
C2H4��g��+4H2O��g����Ͷ�ϱ��뻯ѧ������֮����ͬ���������ַ�Ӧ���ƽ��ת��������ͬ�ġ���ͼ2��֪��T1�¶��£�������ˮ��ƽ�����ֱ�Ϊ6mol��4mol��˵�������ı仯��Ҳ��6mol�����Ը÷�Ӧ��ƽ��ת����Ϊ50%.����ʼ״̬�������Ͷ�����̼�����ʵ����ֱ�Ϊ12mol��4mol����Ӧ���ƽ����Է�������Ϊ![]() ����ƽ��״̬ʱ��CO2��H2��C2H4��H2O�����ʵ����ֱ�Ϊ2mol��6mol��1mol��4mol��ƽ��ʱ�����ƽ����Է�������Ϊ
����ƽ��״̬ʱ��CO2��H2��C2H4��H2O�����ʵ����ֱ�Ϊ2mol��6mol��1mol��4mol��ƽ��ʱ�����ƽ����Է�������Ϊ![]() ���������ʼ״̬��ƽ��ʱ�����ƽ������������İٷ���Ϊ
���������ʼ״̬��ƽ��ʱ�����ƽ������������İٷ���Ϊ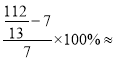 23.1% ��
23.1% ��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�