题目内容
19.下列各组离子中,能在溶液中大量共存的是( )| A. | Ba2+ Cl- Na+ SO42- | B. | Ag+ NO3- K+ CO32- | ||
| C. | Cu2+ Cl- Ag+ OH- | D. | Na+ OH- K+ SO42- |
分析 A.钡离子与硫酸根离子反应生成硫酸钡沉淀;
B.银离子与碳酸根离子反应生成碳酸银沉淀;
C.银离子与氯离子、氢氧根离子反应,铜离子与氢氧根离子反应生成氢氧化铜沉淀;
D.Na+、OH-、K+、SO42-之间不反应,能够大量共存.
解答 解:A.Ba2+、SO42-之间反应生成难溶物硫酸钡,在溶液中不能大量共存,故A错误;
B.Ag+、CO32-之间反应生成碳酸银沉淀,在溶液中不能大量共存,故B错误;
C.Cu2+、Ag+与OH-之间发生反应,Cl-、Ag+之间反应生成难溶物氯化银,在溶液中不能大量共存,故C错误;
D.Na+、OH-、K+、SO42-之间不发生反应,在溶液中能够大量共存,故D正确;
故选D.
点评 本题考查离子共存的正误判断,为高考的高频题,属于中等难度的试题,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间等;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.正丁烷的一氯代物有几种( )
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
10.在①钾盐 ②铵盐 ③硝酸盐 ④硫酸盐 ⑤盐酸盐 ⑥碳酸盐中,均能溶于水的一组盐是( )
| A. | ①②⑤ | B. | ②③④ | C. | ①②③ | D. | ①③⑥ |
14.下列离子方程式正确的是( )
| A. | NaHSO3溶液与NaOH溶液反应:HSO${\;}_{3}^{-}$+OH-=SO${\;}_{3}^{2-}$+H2O | |
| B. | 少量二氧化碳通入足量的NaOH溶液:CO2+OH-=HCO${\;}_{3}^{-}$ | |
| C. | Fe与盐酸反应产生H2:2Fe+6H+=2Fe3++3H2↑ | |
| D. | 氨水和醋酸溶液混合NH3•H2O+CH3COOH=NH${\;}_{4}^{+}$+H2O |
4.下列不能用勒夏特列原理解释的是( )
| A. | 棕红色NO2加压后颜色先变深后变浅 | |
| B. | Fe(SCN)3溶液中加入固体KSCN后颜色变深 | |
| C. | 氯水宜保存在低温、避光条件下 | |
| D. | SO2催化氧化成SO3的反应,往往加入过量的空气 | |
| E. | 打开易拉罐有大量气泡冒出 | |
| F. | 加催化剂,使氮气和氢气在一定条件下转化为氨气 |
9.下列叙述正确的是( )
| A. | ${\;}_{8}^{16}$O2和${\;}_{8}^{18}$O2互为同位素,化学性质相似 | |
| B. | C(石墨,s)=C(金刚石,s)△H>0,所以石墨比金刚石稳定 | |
| C. | 明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同 | |
| D. | 常温下,pH=1的水溶液中Na+、NO3-、HCO3-、Fe2+可以大量共存 |
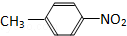 和
和