题目内容
【题目】儿种短周期元素的原子半径及主要化合价如下表
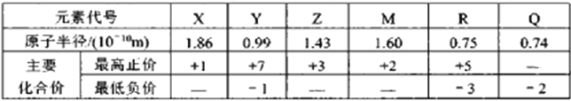
下列说法不正确的是
A. 由元素X和Q组成的化合物可能含有共价键
B. X、Z、R的最高价氧化物对应水化物可彼此反应
C. 离子半径:r(M2-)<r(R3-)
D. Z和Y形成的化合物为离子化合物
【答案】D
【解析】
根据主族元素最高正价=最外层电子数,最低负价的绝对值=8-最外层电子数,还有原子半径的周期性变化规律,可以判断出X: Na,Y:Cl,Z:Al,M:Mg,R:N,Q:O。
A.由元素X(Na)和Q(O)组成的化合物是Na2O或者Na2O2,Na2O2中含有共价键,A不符合题意;
B.X、Z、R的最高价氧化物对应水化物分别是NaOH、Al(OH)3、HNO3,由于氢氧化铝为两性氢氧化物,既可以与强碱反应,也可以与强酸反应,B不符合题意;
C.Mg2+和N3-核外电子排布相同,核电荷数越大吸电子能力越强,半径越小,C不符合题意;
D.Z和Y形成的化合物AlCl3为共价化合物,D符合题意;
答案:D。

练习册系列答案
相关题目