题目内容
9.下列各组物质中,前者为强电解质,后者为弱电解质的是( )| A. | 硫酸,二氧化硫 | B. | BaCO3,氨水 | C. | 盐酸,酒精 | D. | 熔融的氯化钾,水 |
分析 电解质是指在水溶液或熔化状态下都能导电的化合物;强电解质在水溶液或熔融状态下,能完全电离成离子的电解质;弱电解质为:在水溶液里部分电离的电解质,包括弱酸、弱碱、水与少数盐,据此即可解答.
解答 解:A.硫酸在水溶液中能够完全电离为强电解质,二氧化硫本身不能电离,属于非电解质,故A不选;
B.碳酸钡熔化状态下能完全电离,属于强电解质,氨水为混合物,既不是电解质,也不是非电解质,故B不选;
C.盐酸为混合物,既不是电解质,也不是非电解质,故C不选;
D.熔融的氯化钾能够完全电离,属于强电解,水只能部分电离,属于弱电解质,故D选;
故选:D.
点评 本题考查了电解质强弱的判断,熟悉相关概念是解题关键,题目难度不大.

练习册系列答案
相关题目
19.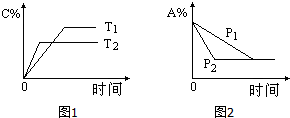 可逆反应:aA(g)+bB(s)?cC(g)+d D(g),当其他条件不变时,反应过程中某物质在混合物中的百分含量与温度(T)、压强(P)的关系如图所示,下列判断正确的是( )
可逆反应:aA(g)+bB(s)?cC(g)+d D(g),当其他条件不变时,反应过程中某物质在混合物中的百分含量与温度(T)、压强(P)的关系如图所示,下列判断正确的是( )
 可逆反应:aA(g)+bB(s)?cC(g)+d D(g),当其他条件不变时,反应过程中某物质在混合物中的百分含量与温度(T)、压强(P)的关系如图所示,下列判断正确的是( )
可逆反应:aA(g)+bB(s)?cC(g)+d D(g),当其他条件不变时,反应过程中某物质在混合物中的百分含量与温度(T)、压强(P)的关系如图所示,下列判断正确的是( )| A. | T1<T2 △H>0 | B. | T1>T2 △H<0 | C. | P1<P2 a=c+d | D. | P1<P2 a+b=c+d |
20.下列叙述错误的是( )
| A. | 甲苯能使酸性高锰酸钾溶液褪色而甲烷不能 | |
| B. | 1.6g甲烷完全燃烧生成二氧化碳和水,转移的电子数为0.8NA(NA为阿伏加德罗常数) | |
| C. | 1mol苯恰好与3mol H2完全加成,说明一个苯分子中有三个碳碳双键 | |
| D. | 烷烃的通式为CnH2n+2,则n=7,主链上有5个碳原子的烷烃共有五种 |
17.恒温下某密闭容器中充入2mol SO2和1mol O2发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0,并达到平衡状态.下列说法中正确的是( )
| A. | 若容器体积不变,充入O2,平衡向右移动,O2的转化率一定增大 | |
| B. | 若容器体积不变,充入Ar,容器内压强增大,平衡向右移动 | |
| C. | 若容器体积不变,升高温度,平衡向左移动,平衡常数K减小 | |
| D. | 若容器压强不变,再充入1 mol SO2和0.5 mol O2,达到新平衡时c(SO2)增大 |
4.下列有关说法错误的是( )
| A. | H2O2、Na2O2都属于过氧化物、都存在非极性共价键 | |
| B. | H2O2做漂白剂是利用其强氧化性,漂白原理与HClO类似但与SO2不同 | |
| C. | 双氧水是绿色氧化剂,可作医疗消毒剂 | |
| D. | H2O2既有氧化性又有还原性,1molH2O2在参加反应时一定转移2mol电子 |
18.珍爱生命,远离毒品.以下是四种毒品的结构简式,下列有关说法正确的是( )
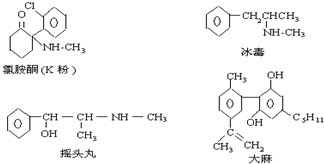

| A. | K粉的分子式为C13H17ClNO | |
| B. | 这四种毒品都属于芳香烃 | |
| C. | 摇头丸不可能发生加成反应 | |
| D. | 1mol大麻可与1mol Br2发生加成反应 |
19.有人设想合成具有以下结构的烃分子,下列说法不正确的是( )
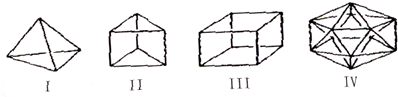

| A. | Ⅳ不可能合成得到 | B. | Ⅱ与苯互为同分异构体 | ||
| C. | Ⅲ(立方烷)的六氯代物共有3种 | D. | Ⅰ中各键之间夹角为109°28′ |

 (1)一个国家乙烯工业的发展水平,已成为衡量这个国家石油化学工业水平的重要标志之一.请列举出乙烯的两种重要用途:①生产聚乙烯,②果实催熟;
(1)一个国家乙烯工业的发展水平,已成为衡量这个国家石油化学工业水平的重要标志之一.请列举出乙烯的两种重要用途:①生产聚乙烯,②果实催熟;