题目内容
【题目】在容积固定的密闭容器中,对于反应2SO2(g)+O2(g)![]() 2SO3(g)ΔH<0。下列判断正确的是 ( )
2SO3(g)ΔH<0。下列判断正确的是 ( )
A. 增大反应体系的压强,平衡后SO2的浓度、转化率、体积分数都增加
B. 当单位时间内消耗SO2的物质的量和生成SO3的物质的量相同时,反应达到平衡状态
C. 升高温度,平衡向左移动
D. 充入SO3气体,体系压强增大,平衡向右移动
【答案】C
【解析】该反应为气体体积减小的反应,增大反应体系的压强,平衡正向移动。则平衡后SO2的浓度、体积分数都减小,转化率增加,A项错误;单位时间内消耗SO2的物质的量和生成SO3的物质的量相同时,均为正向反应速率,不能判定平衡,B项错误;因该反应为放热反应,升高温度平衡向吸热反应的方向移动,即向左移动,C项正确;充入SO3气体,生成物浓度增大,平衡向左移动,D项错误。

【题目】目前,我国是最大的钢铁生产国,钢铁是国民经济的基础产业,铁及其化合物的应用也越来越广泛。回答下列问题:
(1)画出铁的原子结构示意图:______________。
(2)工业炼铁时常用CO还原铁矿粉,已知:
① Fe2O3(s) + 3CO(g)=2Fe(s)+ 3CO2(g) △H=-24.8 kJ/mol
② Fe3O4(S)+CO(g)=-3FeO(g)+CO2(g) △H= +19.4 kJ/mol
③ FeO(s)+CO(g)=Fe(s)+CO2(g) △H= -11.0 kJ/mol
则反应3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)的△H= ________。
(3)Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) 反应温度与K的关系如右表:
反应温度/℃ | 1000 | 1150 | 1300 |
平衡常数K | 64 | 50.7 | 42.9 |
恒温1000℃在体积为10L的恒容密闭容器中加入0.1molFe2O3和0.1molCO,气体混合物中CO2的体积分数φ(CO2)随时间t的变化关系如图所示。
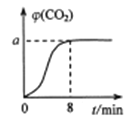
①前 8minCO 的反应速率为_______;平衡时a=____。
②若再向平衡混合物中加入0.01molCO 和0.02molCO2,平衡_______移动;若要使平衡混合气中CO2的体积分数增大,下列措施可行的是_______(填标号)。
A.增大Fe2O3用量 B.增大压强 C.降低温度 D.向容器中再充入少量CO
(4)纳米级的Fe3O4在催化剂、造影成像、药物载体、靶向给药等领域都有很好的应用前景,工业生产中常用“共沉淀法”来制备。将FeCl2和FeCl3按一定比例配成混合溶液,用NaOH溶液作为沉淀剂,在特定条件下即可制得纳米级的Fe3O4,反应的离子方程式是_____,在实际生产中Fe2+和Fe3+反应用量比常是2:3,甚至1:1,为什么?________。
(5)纳米铁粉可用于除去废水中的NO3-,反应的离子方程式为:4Fe+ NO3-+ 10H+=4Fe2++NH4++3H2O。研究发现,若pH偏低将会导致NO3-的去除率下降,其原因是________;若加入少量Cu2+,废水中NO3-的去除速率大大加快,可能的原因是_____________。