题目内容
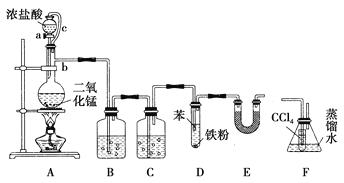
【题目】(题文)某实验小组利用如图装置合成氯苯(支撑用的铁架台部分省略)并通过一定操作提纯氯苯。
反应物和产物的相关数据列表如下:
密度/g·cm-3 | 沸点/℃ | 水中溶解性 | |
苯 | 0.879 | 80.1 | 微溶 |
氯苯 | 1.11 | 131.7 | 不溶 |
请按要求回答下列问题。
(1)仪器b的名称是________。
(2)A装置中制备Cl2的离子方程式为______________________________。
(3)氯气在通入D之前需净化干燥,则装置C中所加试剂的名称为________。
(4)D中通入氯气后,先看到苯呈黄色,片刻试管液面上方有白雾产生,装置E的作用是________。
(5)为证明氯气和苯发生的是取代反应而不是加成反应,该小组用装置F说明,则装置F置于______之间(填字母),F中小试管内CCl4的作用是________,还需使用的试剂是________。
(6)D中混合物经过滤除铁、加水及NaOH溶液洗涤、无水氯化钙干燥等分离操作后得粗氯苯,粗氯苯中还含有的主要杂质为________,要进一步提纯,下列操作中必需的是________(填入正确选项前的字母)。
A.重结晶 B.分液 C.萃取 D.蒸馏
(7)已知D中加入5 mL苯,经过提纯后收集到氯苯3.0g,则氯苯的产率为________%(保留三位有效数字)。
【答案】蒸馏烧瓶MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O浓硫酸除去Cl2和HCl气体,防止大气污染D、E除去Cl2硝酸酸化的硝酸银溶液苯D47.3
Mn2++Cl2↑+2H2O浓硫酸除去Cl2和HCl气体,防止大气污染D、E除去Cl2硝酸酸化的硝酸银溶液苯D47.3
【解析】
(1)根据装置图,仪器b为蒸馏烧瓶,故答案为:蒸馏烧瓶;
(2)A中发生反应为二氧化锰与盐酸反应生成氯化锰、氯气与水,反应离子方程式为:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O,故答案为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O,故答案为:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(3)制备的利用中含有HCl、水蒸汽,用饱和食盐水除去HCl,用浓硫酸吸收水蒸汽,先除去HCl,再进行干燥,故C装置中盛放的试剂为浓硫酸,故答案为:浓硫酸;
(4)D中反应生成氯苯与HCl,未反应的氯气、HCl会污染环境,需要进行尾气处理,故装置E的作用是除去氯气和氯化氢气体,防止污染大气,故答案为:除去氯气和氯化氢气体,防止污染大气;
(5)如果苯和氯气发生的是取代反应,则有HCl生成,如果发生的是加成反应,则无HCl生成,用硝酸酸化的硝酸银溶液检验HCl,装置F应介于D、E之间,由于氯气与硝酸银溶液也会发生反应生成氯化银沉淀,故四氯化碳溶液的作用是除去氯气,故答案为:D和E;除去氯气;硝酸酸化的硝酸银溶液;
(6)粗氯苯中含有未反应的苯,故主要杂质为苯,苯与氯苯互溶,其沸点相差较大,故利用蒸馏的方法将其分离,故答案为:苯;D。
(7)5mL苯的质量为5mL×0.879g/mL=4.395g,则理论上得到氯苯的质量为![]() ×112.5g/mol≈6.33g,故氯苯的产率为
×112.5g/mol≈6.33g,故氯苯的产率为![]() ×100%=47.3%,故答案为:47.3。
×100%=47.3%,故答案为:47.3。