题目内容
15.限用物理方法除去以下物质中的杂质或物质的分离.固体:氯化银中的氯化钠溶解、过滤;硝酸钾中的氯化钠重结晶法;氯化钠中铁屑磁铁;氯化钠中的碘升华;液体:溴水中的溴和水萃取;氯化钠溶液中的水蒸发;乙醇中水蒸馏
气体:空气中提取氮气液化.
分析 氯化钠易溶于水,溶解度与硝酸钾随温度的变化不同,碘易升华;溴易溶于有机溶剂,沸点不同的液体混合物可用蒸馏的方法分离;氮气沸点较低,可用分离液态空气法分离.
解答 解:氯化银不溶于水,可用溶解、过滤的方法除去氯化钠;硝酸钾和氯化钠的溶解度随温度变化不同,可用重结晶法分离;用磁铁除去氯化钠的铁屑;碘易升华,可用升华的方法分离碘;溴易溶于有机溶剂,可用萃取的方法分离;用蒸发的方法除去氯化钠中的水;乙醇和水的沸点不同,可用蒸馏的方法分离;氮气的沸点较低,可用分离液态空气法分离.
故答案为:溶解、过滤;重结晶法;磁铁;升华;萃取;蒸发;蒸馏;液化.
点评 本题考查物质的分离、提纯,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质的异同,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5.当光束通过下列分散系时,不能产生丁达尔效应的是( )
| A. | 稀豆浆 | B. | 淀粉胶体 | C. | 氢氧化钠溶液 | D. | 氢氧化铁胶体 |
6.如果用●代表原子实(原子实是原子除去最外层电子后的剩余部分),小黑点代表未用于形成共价键的最外层电子,一条短线代表一对共用电子对.如F2或Cl2均可表示为 .图甲和图乙所表示的有机分子依次是( )
.图甲和图乙所表示的有机分子依次是( )
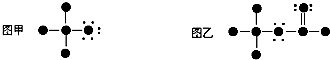
 .图甲和图乙所表示的有机分子依次是( )
.图甲和图乙所表示的有机分子依次是( )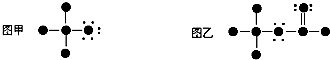
| A. | CCl3H CF3COOH | B. | CH3Cl CH3COOH | ||
| C. | CH3FHCOOCH3 | D. | CH3OH CH2OHCHO |
3.能用溶解、过滤、蒸发、结晶分离的一组混合物是( )
| A. | 酒精和水 | B. | 氯化钠和碳酸钠 | ||
| C. | 碳酸钙和二氧化锰 | D. | 碳酸钙和氯化钠 |
10.相同温度和压强下.下列气体密度最小的是( )
| A. | CO2 | B. | NO2 | C. | SO2 | D. | NH3 |
7.下列表示对应反应的离子方程式正确的是( )
| A. | 向稀 HNO3 中滴加 Na2SO3 溶液:SO32-+2H+═SO2↑+H2O | |
| B. | 双氧水中加入稀硫酸和KI溶液:H2O2+2I-+2H+=I2+2H2O | |
| C. | 向 Al2(SO4)3 溶液中加入过量 NH3•H2O:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O |
4.在一定条件下,下列微粒的还原性顺序为Cl-<Br-<Fe2+<I-<SO2,由此判断以下各反应在溶液中不能发生的是( )
| A. | 2Br-+4H++SO${\;}_{4}^{2-}$═SO2+Br2+2H2O | |
| B. | 2Fe3++SO2+2H2O═2Fe2++SO${\;}_{4}^{2-}$+4H+ | |
| C. | 2Fe2++Cl2═2Fe3++2Cl- | |
| D. | I2+SO2+2H2O═4H++SO${\;}_{4}^{2-}$+2I- |
11.下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:Ar(填具体元素符号或化学式,下同),非金属性最强的元素是:F.
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是:HClO4,碱性最强的化合物的化学式是:KOH.
(3)最高价氧化物是两性氧化物的元素是:Al;写出它的最高价氧化物与氢氧化钠反应的离子方程式:Al2O3+2OH-=2AlO2-+H2O.
(4)④与⑧形成的化合物的电子式是: ,该化合物所含化学键类型是:离子键(填“共价键”或“离子键”).
,该化合物所含化学键类型是:离子键(填“共价键”或“离子键”).
(5)试设计实验方案比较④与⑤的化学性质(金属性),有关实验步骤、现象和结论填入下表
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 4 | ⑩ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是:HClO4,碱性最强的化合物的化学式是:KOH.
(3)最高价氧化物是两性氧化物的元素是:Al;写出它的最高价氧化物与氢氧化钠反应的离子方程式:Al2O3+2OH-=2AlO2-+H2O.
(4)④与⑧形成的化合物的电子式是:
 ,该化合物所含化学键类型是:离子键(填“共价键”或“离子键”).
,该化合物所含化学键类型是:离子键(填“共价键”或“离子键”).(5)试设计实验方案比较④与⑤的化学性质(金属性),有关实验步骤、现象和结论填入下表
| 实验步骤 | 实验现象与结论 |
| . |