题目内容
【题目】X、Y、Z为短周期元素的单质,U、V为它们的化合物,这些物质之间的关系右图所示,其中反应条件和某些产物己经略去:
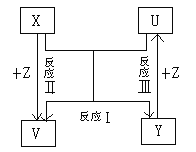
(1)如果X、Y的组成元素是同主族的。
①若已知V是水:写出反应Ⅰ的化学反应方程式:_____________________。
②若已知U、V均为氧化物:则
a.中国北京曙光公司研制出了第一款具有我国完全自主:
知识产权的高性能CPU芯片——“龙芯”Ⅰ号。“龙芯”(芯片)的主要化学成分是Y,该材料的化学式是:________ ;
b.计算机长距离联网使用的传输速度快、信息量大的线路,使用的材料的主要化学成分是U,该材料的名称是:________;
c.这种材料埋在地下时,如果裸露在碱性土壤中,结果会断路,用离子方程式说明原因__________。
(2)如果X、Y的组成元素不同主族时,若Z是通常情况下密度最小的物质,则反应Ⅰ的化学反应方程式:_______________________。
【答案】 H2S+O2=2S+2H2O Si 光导纤维(或光纤) SiO2+2OH-=SiO32-+H2O 2F2+2H2O=4HF+O2 或 3O2+4NH3![]() 2N2+6H2O
2N2+6H2O
【解析】X、Y、Z是短周期元素的单质,U、V是它们的化合物,
(1)如果X、Y组成元素是同主族元素时,符合“U+X=V+Y”的反应方程式,①U+X=V+Y为置换反应,若V为水,X、Z为氢气、氧气,如果X是氢气,氢气和化合物发生置换反应不能生成Na,所以X不是氢气,应该是氧气,则Y是S,Z为氢气,所以A是H2S,则该反应方程式为2H2S+O2=2S+2H2O;②+X=V+Y为置换反应,若已知U、V均为氧化物,X、Y、Z为单质,X和U发生置换反应生成Y,则X具有还原性,“龙芯”(芯片)的主要化学成分是Y,则Y是Si,X为C、Y为Si,U为SiO2、V为CO,U的名称是二氧化硅;二氧化硅是酸性氧化物,能与碱反应,反应的离子方程式为 SiO2+2OH-=SiO32-+H2O;(2)X、Y组成元素不是同主族元素时,若Z是通常情况下密度最小的物质,Z是氢气。则符合条件的可以是氧气和氨气反应生成氮气和水,即X是氧气,U是氨气,V是水,Y是氮气;或者X是氟,U是水,V是HF,Y是氧气,因此反应Ⅰ的化学反应方程式为2F2+2H2O=4HF+O2或3O2+4NH3![]() 2N2+6H2O。
2N2+6H2O。

【题目】Ⅰ.下列气体的制备和性质实验中,由现象得出的结论正确的是________
选项 | 试剂 | 试纸或试液 | 现象 | 结论 |
A | 浓氨水、生石灰 | 红色石蕊试纸 | 变蓝 | NH3为碱性气体 |
B | 浓盐酸、浓硫酸 | 蓝色石蕊试纸 | 变红 | HCl为酸性气体 |
C | 亚硫酸钠、硫酸 | 品红试液 | 褪色 | SO2具有还原性 |
D | 浓盐酸、二氧化锰 | 淀粉碘化钾试液 | 变蓝 | Cl2具有氧化性 |
Ⅱ.CO2是重要的化工原料,也是应用广泛的化工产品。CO2与过氧化钠或超氧化钾反应可产生氧气。完成下列计算:
(1)CO2通入氨水生成NH4HCO3, NH4HCO3很容易分解。 2.00mol NH4HCO3完全分解,分解产物经干燥后的体积为________L(标准状况)。
(2)某H2中含有2.40 molCO2,该混合气体通入2.00LNaOH溶液中,CO2被完全吸收。如果NaOH完全反应,该NaOH溶液的浓度为__________________(填浓度范围)。
(3)CO2和 KO2 有下列反应:4KO2+2CO2=2K2CO3+3O2
4KO2+4CO2+2H2O=4K2HCO3+3O2
若9 mol CO2在密封舱内和KO2反应后生成9 molO2,则反应前密封舱内H2O的物质的量应该是______________。