题目内容
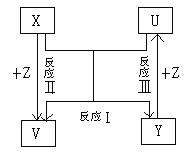
【题目】短周期元素 X、Y、Z 在周期表中位置如右图。下列说法正确的是( )

A. 若 X 通过共用三对电子可形成 X2 分子,Z 在周期表中的位置是第三周期Ⅵ族
B. 若 X、Y、Z 都是金属,则它们的最高价氧化物的水化物都是强碱
C. 若它们原子最外层电子数之和为 13,则它们均为非金属元素
D. 若 X、Y、Z 都是非金属,则三者形成的简单氢化物中,Z 的氢化物沸点 最高
【答案】C
【解析】A.若 X 通过共用三对电子可形成 X2 分子,则X为氮元素,Z 为S元素,在周期表中的位置是第三周期ⅥA族,故A错误;B.若 X、Y、Z 都是金属,其中X如为Be,则Y为Mg、Z为Al,它们的最高价氧化物的水化物均不是强碱,故B错误;C.若它们原子最外层电子数之和为 13,则X为C、Y为Si、Z为P,均为非金属元素,故C正确;D.若 X、Y、Z 都是非金属,如X为O、Y为S、Z为Cl,因H2O分子间存在氢键,其沸点是三者形成的简单氢化物中最高的,故D错误;答案为C。

练习册系列答案
相关题目