题目内容
下列有关金属腐蚀与防护的说法正确的是( )
| A.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阴极的阳极保护法 |
| B.当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
| C.纯银器表面在空气中因化学腐蚀渐渐变暗 |
| D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
C
解析试题分析:在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法,A不正确;金属性是铁>锡,所以当镀锡铁制品的镀层破损时,铁易被腐蚀,选项B不正确;发生电化学腐蚀时,金属应不纯,则纯银器主要发生化学腐蚀,故选项C正确;防止金属被氧化,金属应连接电源的负极,如连接正极,加剧腐蚀,故D不正确,答案选C。
考点:考查金属的腐蚀与防护
点评:该题是高考中的常见题型,属于基础性试题的考查,难度不大。侧重对学生基础知识的巩固和训练。答题时注意把握金属腐蚀的原理和原电池以及电解池的工作原理,然后结合题意灵活运用即可。

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案
相关题目
电解尿素[ CO(NH2)2]的碱性溶液制氢的装置示意图如图(电解池中隔膜仅阻止气体通过,a、b极均为惰性电极)。下列说法正确的是
| A.电解时,b极是阴极放出H2,发生氧化反应 |
| B.溶液中OH—逐渐向b极移动 |
C.电解时,a极的电极反应式为: |
| D.若在b极产生标况下224mL氢气,则消耗尿素2g |
下列叙述正确的是
| A.用饱和NaHCO3溶液可以将混在CO2气体中的HCl除去 |
| B.能使润湿的淀粉KI试纸变蓝的气体一定是Cl2 |
| C.某“海水”电池的总反应为:5MnO2+2Ag+2NaCl==Na2Mn5O10+2AgCl,每生成1 mol Na2Mn5O10转移2 mol电子 |
| D.在铁制品上镀铜时,铁制品作电镀池的阳极,铜盐为电镀液 |
用铜片、银片、Cu (NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U型管)构成一个原电池。以下有关该原电池的叙述正确的是
①在外电路中,电流由铜电极流向银电极 ②正极反应为:Ag++e-=Ag
③实验过程中取出盐桥,原电池仍继续工作
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同
| A.①② | B.②③ | C.②④ | D.③④ |
由于具有超低耗电量、寿命长的特点,LED产品越来越受人欢迎。下图是氢氧燃料电池驱动LED发光的装置。下列有关叙述正确的是( )
| A.a处通人氧气,b处通人氢气 |
| B.该装置中只涉及两种形式的能量转化 |
| C.电池正极电极反应式为O2+2H2O+4e-﹦4OH- |
| D.P一型半导体连接的是电池负极 |
如下图是工业电解饱和食盐水的装置示意图,下列有关说法中不正确的是( )
| A.装置中出口①处的物质是氯气,出口②处的物质是氢气 |
| B.该离子交换膜只能让阳离子通过,不能让阴离子通过 |
C.装置中发生反应的离子方程式为:2Cl-+2H+ Cl2↑+H2↑ Cl2↑+H2↑ |
| D.该装置是将电能转化为化学能 |
利用生活中常见的材料可以进行很多科学实验,甚至制作出一些有实际应用价值的装置来.下图就是一个用废旧材料制作的可用于驱动玩具的电池的示意图.该电池工作时,有关说法正确的是 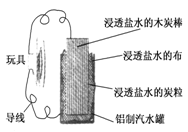
| A.炭棒应与玩具电机的负极相连 |
| B.炭粒和炭棒上发生的反应为:O2+4e-=2O2- |
| C.铝罐将逐渐被腐蚀 |
| D.该电池工作一段时间后炭棒和炭粒的质量会减轻 |

