题目内容
1.金属铁是应用广泛,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物.(1)要确定铁的某氯化物FeClx的化学式,可利用离子交换和滴定的方法.实验中称取3.25g的FeClx样品,溶解后先进行阳离子交换预处理,再通过含有饱和OH-的阴离子交换柱,使Cl-和OH-发生交换.交换完成后,流出溶液的OH-用1.0mol•L-1的盐酸中和滴定,正好中和时消耗盐酸60.0mL.计算该样品中氯的物质的量,并求出FeClx中x的值:n(Cl)=n(H+)=n(OH-)=0.0250L×0.80 mol•L-1=0.020 mol,1.08g FeClx样品中含有氯离子物质的量为$\frac{1.08g}{(56+35.5x)g/mol}$mol,解得x=3(列出计算过程).
(2)现有一含有FeCl2和FeCl3的混合物样品,采用上述方法测得n(Fe):n(Cl)=1:2.8,则该样品中FeCl3的物质的量分数为80%.
(3)把SO2气体通入FeCl3溶液中,发生反应的离子方程式为SO2+2Fe3++H2O=SO42-+2Fe2++4H+.
(4)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料.FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O;与MnO2-Zn电池类似,K2FeO4-Zn也可以组成碱性电池,其中Zn极的电极反应式为3Zn-6e-+6OH-=3Zn(OH)2,K2FeO4的电极反应式为2FeO42-+6e-+8H2O=2Fe(OH)3+10OH-.
分析 (1)根据离子交换关系中n(OH-)=n(Cl-)=n(H+),再根据1.08g FeClx中氯离子物质的量计算x值;
(2)根据元素守恒计算氯化亚铁和氯化铁物质的量之比,进而计算氯化铁质量分数;
(3)SO2与FeCl3溶液反应生成亚铁离子和硫酸根离子;
(4)用FeCl3与KClO在强碱性条件下反应制取K2FeO4,反应的离子方程式为:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O;
K2FeO4-Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,负极为锌失电子发生氧化反应.
解答 解:(1)n(Cl)=n(H+)=n(OH-)=0.0250L×0.80 mol•L-1=0.020 mol,1.08g FeClx样品中含有氯离子物质的量为$\frac{1.08g}{(56+35.5x)g/mol}$mol,解得x=3,
故答案为:n(Cl)=n(H+)=n(OH-)=0.0250L×0.80 mol•L-1=0.020 mol,1.08g FeClx样品中含有氯离子物质的量为$\frac{1.08g}{(56+35.5x)g/mol}$mol,解得x=3;
(2)设混合物中FeCl2物质的量为x,FeCl3的物质的量为y,则(x+y):(2x+3y)=1:2.8,得到x:y=1:4,氯化铁物质的量分数=$\frac{4}{1+4}$×100%=80%,
故答案为:80%;
(3)SO2与FeCl3溶液反应生成亚铁离子和硫酸根离子,则反应的离子方程式为:SO2+2Fe3++H2O=SO42-+2Fe2++4H+;
故答案为:SO2+2Fe3++H2O=SO42-+2Fe2++4H+;
(4)用FeCl3与KClO在强碱性条件下反应制取K2FeO4,反应的离子方程式为:2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O;
原电池的正极发生发生还原反应,正极电极反应式为:FeO42-+3eˉ+4H2O=Fe(OH)3+5OH-;负极发生氧化反应,负极电极反应为:Zn-2e-+2OH-=Zn(OH)2,
故答案为:2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O;FeO42-+3eˉ+4H2O=Fe(OH)3+5OH-;3Zn+2FeO42-+8H2O=3Zn(OH)2+2Fe(OH)3+4OH-.
点评 本题考查滴定计算、离子方程式、原电池的工作原理、电极反应式书写等,是对学生综合能力的考查,需要学生具备扎实的基础,难度中等.

 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案| A. | 饱和氯水中 Cl-、NO3-、Na+、SO32- | |
| B. | c(H+)=1.0×10-13mol/L溶液中 C6H5O-、K+、SO42-、Br- | |
| C. | Na2S溶液中 SO42-、K+、Cl-、Cu2+ | |
| D. | pH=12的溶液中 NO3-、I-、Na+、Al3+ |
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| A. | X、Y元素的金属性 X<Y | |
| B. | 一定条件下,W单质可以将Z单质从其氢化物中置换出来 | |
| C. | 一定条件下,Z单质与W的常见单质直接生成ZW2 | |
| D. | Y的最高价氧化物对应的水化物能溶于稀氨水 |
| A. | 分液时,分液漏斗中的上层液体应由上口倒出 | |
| B. | 为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测定 | |
| C. | 制备Fe(OH)3胶体,通常是将Fe(OH)3固体溶于热水中 | |
| D. | 欲配制质量分数为10%的ZnSO4溶液,将l0 g ZnSO4•7H2O溶解在90 g水中 |
| A. | 100mL0.5mol•L-1MgCl2溶液 | B. | 200mL0.25mol•L-1AlCl3溶液 | ||
| C. | 50mL1mol•L-1NaCl溶液 | D. | 25mL0.5mol•L-1HCl溶液 |
 利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.B极区电解液为LiOH溶液(填化学式),阳极电极反应式为2Cl--2e-=Cl2↑,电解过程中Li+向B电极迁移(填“A”或“B”).
利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.B极区电解液为LiOH溶液(填化学式),阳极电极反应式为2Cl--2e-=Cl2↑,电解过程中Li+向B电极迁移(填“A”或“B”).
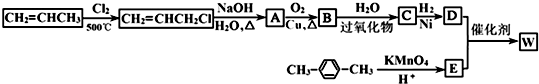
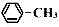 $→_{H+}^{KMnO_{4}}$
$→_{H+}^{KMnO_{4}}$
 .
.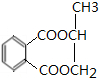 .
.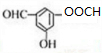 .
. .
.