题目内容
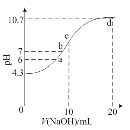
【题目】连二次硝酸(H2N2O2)是一种二元酸,常温下,用0.01mol·L-1的NaOH溶液滴定10mL0.01mol·L-1的H2N2O2溶液,测得溶液pH与NaOH溶液体积的关系如图。常温下,下列各点所对应溶液中微粒物质的量浓度关系正确的是( )
A.a点:c(N2O22-)+c(HN2O2-)-c(Na+)=9.9×10-7mol·L-1
B.b点:c(Na+)>c(N2O22-)+c(HN2O2-)+c(H2N2O2)
C.c点:c(Na+)>c(HN2O2-)>c(N2O22-)>c(H2N2O2)
D.d点:2c(H2N2O2)+c(HN2O2-)+c(H+)=c(OH-)
【答案】D
【解析】
c点:10mL0.01mol·L-1的H2N2O2溶液滴加10mL 0.01mol·L-1的NaOH溶液二者发生反应,生成NaHN2O2溶液,此时pH大于7,则HN2O2水解大于电离,离子浓度大小比较:c(Na+)>c(HN2O2-)>c(H2N2O2) >c(N2O22-);d点:滴加20mL 0.01mol·L-1的NaOH溶液二者发生反应,生成Na2N2O2溶液,存在三大守恒;a和b点的溶质都含有NaHN2O2 和H2N2O2,但是比例不同,在没有明确的量比关系时,只能书写电荷守恒。
A.存在电荷守恒表示为2c(N2O22-)+c(HN2O2-)+ c(OH-)=c(Na+)+c(H+),a点pH=6,故2c(N2O22-)+c(HN2O2-)-c(Na+)=9.9×10-7mol·L-1,A项错误;
B. NaHN2O2的物料守恒表示为 c(Na+)=c(N2O22-)+c(HN2O2-)+c(H2N2O2),b点溶质含有NaHN2O2 和H2N2O2,故c(Na+)<c(N2O22-)+c(HN2O2-)+c(H2N2O2),B项错误;
C. 根据分析,c点:c(Na+)>c(HN2O2-)>c(H2N2O2) >c(N2O22-),C项错误;
D.根据分析, d点的质子守恒可以表示为:2c(H2N2O2)+c(HN2O2-)+c(H+)=c(OH-),D项正确;
答案选D。

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案【题目】三氧化二钴(Co2O3)主要用作颜料、釉料、磁性材料、催化剂和氧化剂等。以含钴废料(主要成分为Co2O3,含有少量MnO2、NiO、Fe3O4)为原料制备Co2O3的流程如下图所示:

已知:
Ⅰ.“酸浸”后的浸出液中含的阳离子有H+、Co2+、Fe3+、Ni2+等。
Ⅱ.部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:
沉淀物 | Fe(OH)3 | Co(OH)2 | Ni(OH)2 |
完全沉淀时的pH | 3.7 | 9.0 | 9.2 |
回答下列问题:
(1)“酸浸”含钴废料的温度不宜过高,原因是_____________。
(2) “酸浸”时发生的主要反应是___________________(写离子方程式)。
(3)某萃取剂对金属离子的萃取率与溶液pH的关系如图所示:
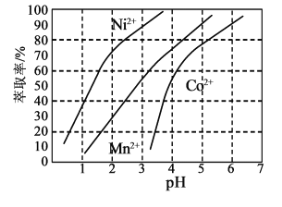
使用该萃取剂时应控制的pH约为____________,理由是_____________。
(4)写出高温煅烧时发生的化学反应方程式___________。
(5)操作1得到的副产品是__________(填名称);
已知该物质的溶液加热到100℃时会变质,该物质的溶解度见下表:
湿度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ |
溶解度 | 70.6 | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 | 88.0 |
操作1是________(填字母)。
a.蒸发结晶 b.降温结晶 c.减压蒸发结晶
(6)有机相提取的Ni2+再生时可用于制备镍氢电池,该电池充电时的总反应为Ni(OH)2+M=NiOOH+MH,则放电时负极的电极反应式为_________________。
【题目】根据杂化轨道理论和价层电子对互斥模型,判断下列分子或者离子的空间构型正确的是
选项 | 分子式 | 中心原子杂化方式 | 价层电子对互斥模型 | 分子或离子的立体构型 |
A | SO2 | sp | 直线形 | 直线形 |
B | HCHO | sp2 | 平面三角形 | 三角锥形 |
C | H3O+ | sp2 | 四面体形 | 平面三角形 |
D | NH4+ | sp3 | 正四面体形 | 正四面体形 |
A. AB. BC. CD. D