题目内容
二甲醚(CH3OCH3)是一种重要的精细化工产品,被认为是二十一世纪最有潜力的燃料(已知:CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(1)△H=-1455KJ/mol).同时它也可以作为制冷剂而替代氟氯代烃.工业上制备二甲醚的主要方法经历了三个阶段:
①甲醇液体在浓硫酸作用下或甲醇气体在催化作用下直接脱水制二甲醚;
2CH3OH
CH3OCH3+H2O
②合成气CO与H2直合成二甲醚:
3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-247kJ/mol
③天然气与水蒸气反应制备二甲醚.以CH4和H20为原料制备二甲醚和甲醇工业流程如下:
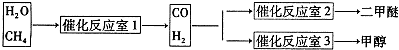
(1)写出CO(g)、H2(g)、O2(g)反应生成CO2(g)和H2O(1)的热化学方程式______.
(2)①方法中用甲醇液体与浓硫酸作用直接脱水制二甲醚,尽管产率高,但是逐步被淘汰的主要原因是______.
(3)在反应室2中,一定条件下发生反应3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)在密闭容器中达到平衡后,要提高CO的转化率,可以采取的措施是______.
A.低温高压B.加催化剂C.增加CO浓度D.分离出二甲醚
(4)在反应室3中,在一定温度和压强条件下发生了反应:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g),△H<0,
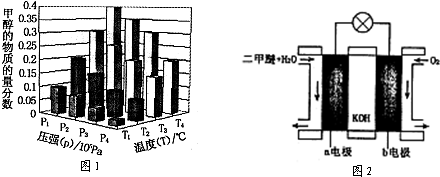
反应达到平衡时,改变温度(T)和压强(P),反应混合物CH3OH“物质的量分数”变化情况如图所示,关于温度(T)和压强(P)的关系判断正确的是______.(填序号).
A.P3>P2 T3>T2 B.P2>P4 T4>T2
C.P1>P3 T1>T3 D.P1>P4 T2>T3
(5)反应室1中发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0写出平衡常数的表达式:______.如果温度降低,该反应的平衡常数______.(填“不变”、“变大”、“变小”)
(6)如图为绿色电源“二甲醚燃料电池”的工作原理示意图.则a电极的反应式为:______.

①甲醇液体在浓硫酸作用下或甲醇气体在催化作用下直接脱水制二甲醚;
2CH3OH
| 催化剂 |
②合成气CO与H2直合成二甲醚:
3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-247kJ/mol
③天然气与水蒸气反应制备二甲醚.以CH4和H20为原料制备二甲醚和甲醇工业流程如下:
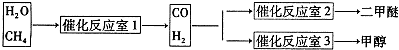
(1)写出CO(g)、H2(g)、O2(g)反应生成CO2(g)和H2O(1)的热化学方程式______.
(2)①方法中用甲醇液体与浓硫酸作用直接脱水制二甲醚,尽管产率高,但是逐步被淘汰的主要原因是______.
(3)在反应室2中,一定条件下发生反应3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)在密闭容器中达到平衡后,要提高CO的转化率,可以采取的措施是______.
A.低温高压B.加催化剂C.增加CO浓度D.分离出二甲醚
(4)在反应室3中,在一定温度和压强条件下发生了反应:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g),△H<0,
反应达到平衡时,改变温度(T)和压强(P),反应混合物CH3OH“物质的量分数”变化情况如图所示,关于温度(T)和压强(P)的关系判断正确的是______.(填序号).
A.P3>P2 T3>T2 B.P2>P4 T4>T2
C.P1>P3 T1>T3 D.P1>P4 T2>T3
(5)反应室1中发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0写出平衡常数的表达式:______.如果温度降低,该反应的平衡常数______.(填“不变”、“变大”、“变小”)
(6)如图为绿色电源“二甲醚燃料电池”的工作原理示意图.则a电极的反应式为:______.
(1)已知①CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(1)△H=-1455KJ/mol;
②3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-247kJ/mol,反应CO(g)+H2(g)+O2(g)=CO2(g)+H2O(1)可以是
(①+②)得到,所以△H=-567.3kJ/mol,故答案为:CO(g)+H2(g)+O2(g)=CO2(g)+H2O(1),△H=-567.3kJ/mol;
(2)浓硫酸具有强的腐蚀性,对设备腐蚀严重,且会伴随反应产物二氧化硫的产生,环境污染严重,并且操作条件恶劣,故答案为:浓硫酸对设备腐蚀严重,环境污染严重,操作条件恶劣;
(3)A.低温高压均能使得化学平衡正向移动,可以提高CO的转化率,故A正确;
B.加催化剂,不会改变转化率,故B错误;
C.增加CO浓度,会使其转化率减小,故C错误;
D.分离出二甲醚,能使得化学平衡正向移动,可以提高CO的转化率,故D正确;
故选AD.
(4)对于反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),△H<0,压强越大,甲醇的物质的量分数则越大,温度越高,甲醇的物质的量分数越小,所以P1>P3、T1>T3,P1>P4、T2>T3,故答案为:CD;
(5)反应CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0的平衡常数的表达式K=
,该反应是吸热的,所以如果温度降低,化学平衡常数减小,故答案为:变小;
(6)燃料电池中,通入燃料二甲醚的电极a是负极,该极上发生失电子的氧化反应,即(CH2)2O-12e-+16OH-=2CO32-+11H2O,
故答案为:(CH2)2O-12e-+16OH-=2CO32-+11H2O.
②3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-247kJ/mol,反应CO(g)+H2(g)+O2(g)=CO2(g)+H2O(1)可以是
| 1 |
| 3 |
(2)浓硫酸具有强的腐蚀性,对设备腐蚀严重,且会伴随反应产物二氧化硫的产生,环境污染严重,并且操作条件恶劣,故答案为:浓硫酸对设备腐蚀严重,环境污染严重,操作条件恶劣;
(3)A.低温高压均能使得化学平衡正向移动,可以提高CO的转化率,故A正确;
B.加催化剂,不会改变转化率,故B错误;
C.增加CO浓度,会使其转化率减小,故C错误;
D.分离出二甲醚,能使得化学平衡正向移动,可以提高CO的转化率,故D正确;
故选AD.
(4)对于反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),△H<0,压强越大,甲醇的物质的量分数则越大,温度越高,甲醇的物质的量分数越小,所以P1>P3、T1>T3,P1>P4、T2>T3,故答案为:CD;
(5)反应CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0的平衡常数的表达式K=
| c(CO)?c3(H2) |
| c(CH4)?c(H2O) |
(6)燃料电池中,通入燃料二甲醚的电极a是负极,该极上发生失电子的氧化反应,即(CH2)2O-12e-+16OH-=2CO32-+11H2O,
故答案为:(CH2)2O-12e-+16OH-=2CO32-+11H2O.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
 SO3(g),K1=20,
SO3(g),K1=20,