题目内容
15.海水中可提取多种化工原料,请按要求回答问题:(1)浩瀚的海洋是一个巨大的宝库,下列物质不需要通过化学变化就能够从海水中获得的是AC.
A.食盐 B.金属钠 C.淡水 D.金属镁 E、碘单质
(2)以电解食盐水为基础制取Cl2等产品的工业称为“氯碱工业”;请写出电解饱和食盐水制取Cl2的化学方程式2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑.
(3)实验室制取氯气的反应原理为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;从下列装置(图1)中选择合适的发生装置用于实验室制取少量氯气b.
(4)实验室中模拟Br-→Br2的转化,可以通过在KBr溶液中滴加少量新制的氯水而实现,请写出化学方程式为:2KBr+Cl2=2KCl+Br2;氯水不稳定,要现用现配,下列吸收氯气制备氯水的装置(图2)最合理的是d.
(5)电解熔融氯化镁所得的镁蒸气冷却后即为固体镁.下列气体中,可以用于冷却镁蒸气的是CE.
A.Cl2 B.N2 C.Ar D.空气 E.H2.

分析 (1)根据从海水制备物质的原理可知,金属单质与非金属单质需要利用化学反应来制取,而食盐可利用蒸发原理,淡水利用蒸馏原理来得到;
(2)电解饱和食盐水生成氯气、氢气和氢氧化钠;
(3)依据反应物状态和反应条件选择合适的装置;
(4)氯气氧化性强于溴,能够置换溴;由于氯气有毒,所以需要对尾气进行吸收;
(5)可以用于冷却镁蒸气应不能与镁反应,据此解答.
解答 解:(1)把海水用蒸馏等方法可以得到淡水,把海水用太阳暴晒,蒸发水分后即得食盐,都不需要化学变化就能够从海水中获得;
故答案为:AC;
(2)电解饱和食盐水生成氯气、氢气和氢氧化钠,化学方程式:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑,
故答案为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑;
(3)MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,可知反应物为固体与液体加热反应,应选择装置:b;
故答案为:b;
(4)氯气与溴化钾反应生成氯化钾和溴单质,方程式:2KBr+Cl2=2KCl+Br2;氯气有毒,应注意尾气吸收,以防污染空气,所以装置d最合理;
故答案为:2KBr+Cl2=2KCl+Br2;d;
(5)能和金属镁发生反应的气体:Cl2、N2、空气,不能与金属镁发生反应的气体:Ar、H2,
故答案为:CE.
点评 本题考查了氯气的制备和海水提溴,明确气体制备原理和性质是解题关键,注意发生装置选择的依据,题目难度不大.

练习册系列答案
相关题目
5.25℃时,下列各组离子能在指定溶液中大量共存的是( )
| A. | 无色溶液:K+、Na+、MnO4-、SO42- | |
| B. | pH=11溶液:CO32-、Na+、K+、SO32- | |
| C. | 由水电离的 c(H+)=10-12 mol•L-1,溶液:Cl-、HCO3-、NO3-、Na+ | |
| D. | 酸性溶液:Fe2、NO3-、Cl-、NH4+ |
6.已知,常温下,Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.3×10-17,下列叙述中正确的是( )
| A. | 向AgCl的悬浊液中加入KI溶液,沉淀由白色转化为黄色 | |
| B. | 向AgCl的饱和溶液中加入KCl晶体,有AgCl析出且溶液中c(Ag+)=c(Cl-) | |
| C. | 常温下,AgCl在饱和KCl溶液中的Ksp比在纯水中的Ksp小 | |
| D. | 将0.001 mol•L-1的AgNO3溶液滴入NaCl和NaI的混合溶液中,一定先产生AgI沉淀 |
3.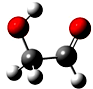 迄今为止科学家在星云中已发现180多种星际分子,寓意着地球上的生命或起源于太空.近年来发现的星际分子乙醇醛球棍模型如图,有关乙醇醛说法错误的是( )
迄今为止科学家在星云中已发现180多种星际分子,寓意着地球上的生命或起源于太空.近年来发现的星际分子乙醇醛球棍模型如图,有关乙醇醛说法错误的是( )
 迄今为止科学家在星云中已发现180多种星际分子,寓意着地球上的生命或起源于太空.近年来发现的星际分子乙醇醛球棍模型如图,有关乙醇醛说法错误的是( )
迄今为止科学家在星云中已发现180多种星际分子,寓意着地球上的生命或起源于太空.近年来发现的星际分子乙醇醛球棍模型如图,有关乙醇醛说法错误的是( )| A. | 有2种含氧官能团 | B. | 能发生银镜反应 | ||
| C. | 与葡萄糖互为同系物 | D. | 与乙酸互为同分异构体 |
20.工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)?Si(s)+4HCl(g);△H=+Q kJ•mol-1(Q>0),某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是( )
| A. | 反应过程中,若增大压强能提高SiCl4的转化率 | |
| B. | 若反应开始时SiCl4为1 mol,则达平衡时,吸收热量为Q kJ | |
| C. | 反应4 min时,若HCl浓度为0.12 mol•L-1,则H2反应速率为0.03 mol•L-1•min-1 | |
| D. | 当反应吸收热量为0.025Q kJ时,生成的HCl通入100 mL 1 mol•L-1的NaOH溶液恰好反应 |
7.欲除去下列物质中混入的少量杂质(括号内物质为杂质),不能达到目的是( )
| A. | 乙酸乙酯(乙酸):加饱和Na2CO3 溶液,充分振荡静置后,分液 | |
| B. | 乙醇(水):加入新制生石灰,蒸馏 | |
| C. | 乙酸(乙醇):加入金属钠,蒸馏 | |
| D. | 苯(液溴):加入NaOH溶液,分液 |
4.元素周期表是学习化学的重要工具,它隐含着许多信息和规律.下面是八种短周期元素的相关信息(已知Be的原子半径为0.089nm)
F原子中无中子,G最高正价为负价绝对值相等,且最外层电子数是次外层的二倍,H元素单质熔色反应呈黄色.
(1)B元素在元素周期表中的位置第三周期ⅢA族.B形成的简单离子的结构示意图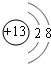 .
.
(2)上述八种元素的最高价氧化物对应的水化物中酸性最强的是HClO4(填化学式).
(3)用电子式表示C,H形成化合物的过程 .
.
(4)H,E形成原子个数比为1:1的化合物中所含化学键类型为离子键、共价键.
(5)F与G形成的最简单的化合物的电子式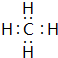 .
.
(6)E的氢化物比C的氢化物的熔沸点高的原因是水分子之间存在氢键,硫化氢分子之间为范德华力,氢键比范德华力更强.
(7)A,B,C,E所形成的简单离子半径由大到小的顺序为S2->O2->Mg2+>Al3+.
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | -1 | -2 |
(1)B元素在元素周期表中的位置第三周期ⅢA族.B形成的简单离子的结构示意图
 .
.(2)上述八种元素的最高价氧化物对应的水化物中酸性最强的是HClO4(填化学式).
(3)用电子式表示C,H形成化合物的过程
 .
.(4)H,E形成原子个数比为1:1的化合物中所含化学键类型为离子键、共价键.
(5)F与G形成的最简单的化合物的电子式
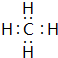 .
.(6)E的氢化物比C的氢化物的熔沸点高的原因是水分子之间存在氢键,硫化氢分子之间为范德华力,氢键比范德华力更强.
(7)A,B,C,E所形成的简单离子半径由大到小的顺序为S2->O2->Mg2+>Al3+.
5.某同学为检验某溶液中是否含有常见的四种无机离子,进行了如图所示的实验操作.其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝.由该实验能得到的正确结论是( )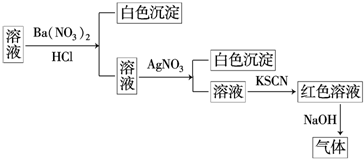

| A. | 原溶液中一定含有SO42- | B. | 原溶液中一定含有NH4+ | ||
| C. | 原溶液中一定含有Cl- | D. | 原溶液中一定含有Fe3+ |
