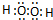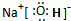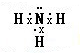题目内容
2.较活泼的金属锌不同浓度的硝酸反应时,可得到不同价态的还原产物,如果起反应的锌和硝酸的物质的量之比为4:10,则硝酸的还原产物可能为( )| A. | NO2 | B. | NO | C. | N2O | D. | NH4NO3 |
分析 锌和稀硝酸发生氧化还原反应,起反应的锌和硝酸的物质的量之比为4:10,假设锌为4mol,生成硝酸锌为4mol,作酸性的硝酸为8mol,则锌与被还原的硝酸的物质的量之比为4:2,则被还原的硝酸为2mol,结合电子的转移数目相等计算.
解答 解:锌和稀硝酸发生氧化还原反应,起反应的锌和硝酸的物质的量之比为4:10,假设锌为4mol,生成硝酸锌为4mol,作酸性的硝酸为8mol,则锌与被还原的硝酸的物质的量之比为4:2,则被还原的硝酸为2mol,
反应后Zn被氧化为+2价,设硝酸还原产物为x价,
则4mol×(2-0)=2mol×(5-x),
x=+1,则还原产物N2O,或NH4NO3,
故选CD.
点评 本题考查氧化还原反应的计算,为高考常见题型和高频考点,侧重于学生的分析能力和计算能力的考查,注意把握电子守恒计算该题,题目难度中等.

练习册系列答案
相关题目
7.某氧原子的质量为a g,12C原子的质量为b g,且NA表示阿佛加德罗常数,下列说法中不正确的是( )
| A. | 氧元素的相对原子质量为$\frac{12a}{b}$ | B. | 1 mol该原子质量为aNAg | ||
| C. | x g该氧原子所含的电子数为$\frac{8x}{a}$ | D. | y g该氧原子的中子数一定为$\frac{8y}{a}$ |
11.下列物质同分异构体数目最少的是( )
| A. | C5H10 | B. | C5H12O | C. | C5H11Br | D. | C5H12 |

 ).实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成乙酰水杨酸,制备的主要反应如图1:操作流程如图2:
).实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成乙酰水杨酸,制备的主要反应如图1:操作流程如图2: .
. +3NaOH
+3NaOH CH3COONa+2H2O+
CH3COONa+2H2O+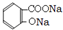 .
.
 CO32-+7H2O.
CO32-+7H2O.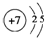 ,C元素在周期表中的位置第三周期ⅥA族.
,C元素在周期表中的位置第三周期ⅥA族. 或
或