题目内容
【题目】实验室用乙醇和浓硫酸反应制备乙烯,化学方程式为:C2H5OH![]() CH2=CH2↑+H2O,接着再用液溴与乙烯反应制备1,2-二溴乙烷。在制备过程中由于部分乙醇与浓硫酸发生氧化还原反应还会产生CO2、SO2,并进而与Br2反应生成HBr等酸性气体。某学习小组用上述三种为原料,组装下列仪器(短接口或橡皮管均己略去)来制备1,2-二溴乙烷
CH2=CH2↑+H2O,接着再用液溴与乙烯反应制备1,2-二溴乙烷。在制备过程中由于部分乙醇与浓硫酸发生氧化还原反应还会产生CO2、SO2,并进而与Br2反应生成HBr等酸性气体。某学习小组用上述三种为原料,组装下列仪器(短接口或橡皮管均己略去)来制备1,2-二溴乙烷
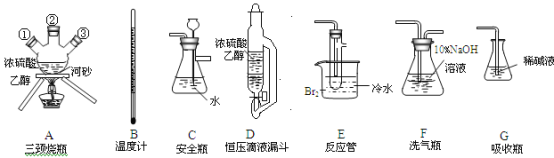
(1)如果气体流向从左到右,正确的连接顺序是:
B经A①插入A中,D接入②;A③接__接__接___接___。
(2)温度计水银球的正确位置是_________。
(3)装置D与分流漏斗相比,其主要优点是_______。
(4)装置C的主要作用是_______,装置F的作用是__________。
(5)在反应管E中进行的主要反应的化学方程式为________。
(6)装置E烧杯中的泠水和反应管内液溴上的水层作用均是_______________。若将装置F拆除,在E中的主要反应为_______。
【答案】C F E G 位于三颈瓶的液体中央 平衡上下压强,使液体顺利滴下 防倒吸 除去三颈瓶中产生的CO2、SO2,吸收挥发的溴蒸汽 CH2=CH2+ Br2![]() BrCH2CH2Br 减少溴的挥发 SO2+Br2+2H2O=H2SO4+2HBr
BrCH2CH2Br 减少溴的挥发 SO2+Br2+2H2O=H2SO4+2HBr
【解析】
(1)根据装置中试剂可知ABD用来制备乙烯,由于生成的乙烯中含有SO2和CO2等气体,在利用乙烯与溴反应之前需要除去。C起到安全瓶的作用,目的是为防止倒吸。E装置用来制备1,2—二溴乙烷,生成的1,2—二溴乙烷中含有溴,利用F装置除杂,最后利用G装置进行尾气处理,则正确的连接顺序是B经A①插入A中,D接入②;A③接C、F、E、G。
(2)温度计测量的是溶液的温度,因此位于三颈瓶的液体中央;
(3)D是恒压漏斗,能保持内外压强相同,则其作用是平衡上下压强,使液体顺利滴下;
(4)根据以上分析可知装置C的主要作用是防倒吸。装置F的作用是除去三颈瓶中产生的CO2、SO2并吸收挥发的溴蒸汽;
(5)E装置用来制备1,2—二溴乙烷,反应的方程式为CH2=CH2+ Br2![]() BrCH2CH2Br。
BrCH2CH2Br。
(6)由于液溴易挥发,则装置E烧杯中的冷水和反应管内液溴上的水层作用均是减少溴的挥发;若将装置F拆除,则SO2易与溴发生氧化还原反应,所以在E中的主要反应为SO2+Br2+2H2O=H2SO4+2HBr。


