题目内容
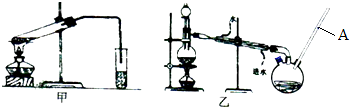
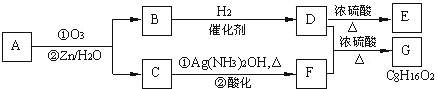
17.某化学课外兴趣小组学生用如图所示的装置探究苯和液溴的反应并制备溴苯.请分析后回答下列问题:
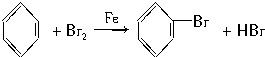
(1)关闭F夹,打开C夹,向装有少量苯的三颈烧瓶的A口加少量液溴,再加入少量铁屑,塞住A口,则三颈烧瓶中发生反应的化学方程式为
 .
.(2)D、E试管内出现的现象分别为石蕊溶液变红;出现淡黄色沉淀.
(3)三颈烧瓶右侧导管特别长,除导气外还起的作用是冷凝回流.
(4)待三颈烧瓶中的反应进行到仍有气泡冒出时松开F夹,关闭C夹,可以看到的现象是与F相连的广口瓶中NaOH溶液流入烧瓶.
(5)反应结束后将三颈烧瓶中的溴苯分离出来的实验方法是分液(铁屑已分离),此时溴苯中还含有少量的苯,除去苯应采用的方法是蒸馏.流,提高原料利用率.
分析 (1)根据苯与溴发生取代反应生成溴苯和溴化氢,从而写出方程式;
(2)反应产生的溴化氢气体遇到石蕊溶液,能石蕊溶液变红色,溴化氢气体通入硝酸银溶液,能产生浅黄色沉淀;
(3)由于苯和液溴都是易挥发的,所以三颈烧瓶右侧导管除导气外还起的作用是冷凝回流作用;
(4)溴化氢极易溶于水,容易发生倒吸;
(5)溴苯与水不互溶,可用分液的方法分开;溴苯与苯是互溶的液体,可用蒸馏的方法分开;
解答 解:(1)苯与溴发生取代反应生成溴苯和溴化氢,反应的方程式为 ,
,
故答案为: ;
;
(2)苯与溴发生取代反应生成溴苯和溴化氢,产生的溴化氢气体遇到石蕊溶液,能石蕊溶液变红色,溴化氢气体通入硝酸银溶液,能产生浅黄色沉淀,所以D试管内出现的现象为石蕊溶液变红,E试管内出现的现象为出现淡黄色沉淀,
故答案为:石蕊溶液变红;出现淡黄色沉淀;
(3)三颈烧瓶右侧导管特别长,除导气外还起的作用是冷凝回流;
故答案为:冷凝回流;
(4)在铁作催化剂的作用下,溴与苯反应生成溴苯、溴化氢,待三口烧瓶中的反应即将结束时(此时气体明显减少),打开F活塞,关闭C活塞,溴化氢通过F进入最左边集气瓶,溴化氢极易溶于水,产生倒吸现象;
故答案为:与F相连的广口瓶中NaOH溶液流入烧瓶;
(5)溴苯不溶于水,分液即可得到溴苯;溴苯与苯互溶,蒸馏即可得到溴苯;
故答案为:分液;蒸馏.
点评 该题是高考中的常见题型,属于中等难度的试题,试题综合性强,难易适中.在注重对学生基础性知识考查和训练的同时,侧重对学生能力的培养和解题方法的指导与训练,有利于培养学生的严谨规范的实验设计能力,也有利于提高学生的学科素养.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
15. 室温下向10mL 0.1mol/L NaOH 溶液中加入0.1mol/L 的一元酸HA 溶液pH 的变化曲线如图所示.下列说法正确的是( )
室温下向10mL 0.1mol/L NaOH 溶液中加入0.1mol/L 的一元酸HA 溶液pH 的变化曲线如图所示.下列说法正确的是( )
 室温下向10mL 0.1mol/L NaOH 溶液中加入0.1mol/L 的一元酸HA 溶液pH 的变化曲线如图所示.下列说法正确的是( )
室温下向10mL 0.1mol/L NaOH 溶液中加入0.1mol/L 的一元酸HA 溶液pH 的变化曲线如图所示.下列说法正确的是( )| A. | a 点所示溶液中c(A-)+c(HA)=0.1mol/L | |
| B. | a、b 两点所示溶液中水的电离程度不同 | |
| C. | pH=7 时,c(Na+)=c(A-)+c(HA) | |
| D. | b 点所示溶液中c(HA)>c(A-) |
8.下列关于化学键的说法中正确的是( )
| A. | 化学键是一种静电引力 | |
| B. | 化学键可以使离子结合,也可以使原子结合 | |
| C. | 只要有旧健的断裂就一定是化学反应 | |
| D. | 氢键是一种化学键 |
9.某溶液中,除水电离出的H+、OH-之外仅含Fe2+、Na+、Al3+、Ba2+、SO42-、NO3-、Cl-中的4种,这4种离子的物质的量均为0.1mol.若向该溶液中加入足量稀硫酸,无沉淀生成但有无色气泡产生.下列说法错误的是( )
| A. | 该溶液中一定不含Ba2+ | |
| B. | 该溶液中一定含Na+ | |
| C. | 无色气体在标准状况下的体积约为2.24L | |
| D. | 若向该溶液中加入足量NaOH溶液,滤出沉淀,洗净灼烧后最多能得8.0g固体 |
7.下列四种演示金属钾与水反应的实验装置,正确的是( )
| A. |  | B. |  | C. |  | D. |  |

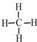 .乙烯的电子式是
.乙烯的电子式是 .将6.72L(标准状况)乙烯和甲烷的混合气通入足量的溴水中,充分反应后,溴水的质量增加了1.4g,原混合气体中乙烯和甲烷的物质的量之比是1:5
.将6.72L(标准状况)乙烯和甲烷的混合气通入足量的溴水中,充分反应后,溴水的质量增加了1.4g,原混合气体中乙烯和甲烷的物质的量之比是1:5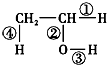 在不同的化学反应中会断裂不同的化学键,请写出下列反应的化学方程式,并指出反应时乙醇分子中断裂的化学键.
在不同的化学反应中会断裂不同的化学键,请写出下列反应的化学方程式,并指出反应时乙醇分子中断裂的化学键.