题目内容
【题目】如下图所示是某品牌饮用矿泉水标签的部分内容。

请认真阅读标签内容,计算:
(1)镁离子的物质的量浓度的最大值_______。
(2)一瓶合格的这种矿泉水中硫酸根离子的物质的量不能超过多少_______?(单位:mol)
【答案】2.04×10-4mol·L-1 7.11×10-5mol
【解析】
根据n=![]() 计算溶质的物质的量,根据c=
计算溶质的物质的量,根据c=![]() 计算溶质的物质的量浓度。
计算溶质的物质的量浓度。
(1)1L矿泉水中镁离子的最大质量为4.9mg,物质的量为![]() =
=![]() mol,
mol,
镁离子的物质的量浓度的最大值为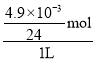 =2.04×104mol/L,
=2.04×104mol/L,
故答案为:2.04×104mol/L;
(2)350mL矿泉水中含有硫酸根离子的最大质量为0.35L×19.5mg/L=6.825mg=6.825×103g,
硫酸根离子的物质的量最大为:n=![]() =
=![]() =7.11×105mol,
=7.11×105mol,
故答案为:7.11×105mol。

练习册系列答案
相关题目
【题目】![]() 、
、![]() 、
、![]() 、
、![]() 为短周期元素,其原子半径、化合价等信息见下表。以下说法一定正确的是( )
为短周期元素,其原子半径、化合价等信息见下表。以下说法一定正确的是( )
元素 |
|
|
|
|
原子半径( | 0.077 | 0.070 | 0.104 | 0.099 |
最高正价或最低负价 | +4 | +5 | -2 | -1 |
A.![]() 与
与![]() 形成的化合物的电子式可表示为
形成的化合物的电子式可表示为![]()
B.![]() 的氢化物能与
的氢化物能与![]() 的氢化物反应,所得产物只含有共价键
的氢化物反应,所得产物只含有共价键
C.![]() 、
、![]() 能分别与氧元素形成多种氧化物
能分别与氧元素形成多种氧化物
D.![]() 处于元素同期中第三周期ⅣA族
处于元素同期中第三周期ⅣA族
【题目】某海水中主要离子的含量如下表,现利用“电渗析法”进行淡化,技术原理如图所示(两端为惰性电极,阳膜只允许阳离子通过,阴膜只允许阴离子通过)。下列有关说法错误的是( )
离子 |
|
|
|
|
|
|
|
含量 | 9360 | 83 | 200 | 1100 | 16000 | 1200 | 118 |

A.甲室的电极反应式为:![]()
B.乙室和丁室中部分离子的浓度增大,淡水的出口为b
C.当戊室收集到![]() (标准状况)气体时,通过甲室阳膜的离子的物质的量一定为
(标准状况)气体时,通过甲室阳膜的离子的物质的量一定为![]()
D.淡化过程中易在戊室形成水垢