题目内容
8.不能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是( )| A. | 加热这两种固体物质,并将生成的气体通入澄清的石灰水中 | |
| B. | 在这两种物质的溶液中加入CaCl2溶液 | |
| C. | 在等物质的量浓度的两种物质的溶液中分别滴加稀盐酸 | |
| D. | 在这两种物质的溶液中加入少量澄清的石灰水 |
分析 Na2CO3和NaHCO3性质不同:①NaHCO3受热分解,②碳酸钙难溶于水,而碳酸氢钙溶于水,③NaHCO3与盐酸反应剧烈,④都能澄清石灰水反应生成碳酸钙沉淀.
解答 解:A.Na2CO3受热不分解,而NaHCO3受热分解,可以鉴别,故A不选;
B.Na2CO3与CaCl2溶液作用产生CaCO3沉淀,而NaHCO3则不与CaCl2溶液反应,无沉淀产生,也可以鉴别,故B不选;
C.向Na2CO3中逐滴加入盐酸时,先无气体产生,当盐酸加入较多时,可产生气体,而向NaHCO3中加入同浓度盐酸,则迅速产生气体,可以通过产生气体的快慢加以鉴别,故C不选;
D.Na2CO3和NaHCO3均可与澄清石灰水反应产生沉淀,现象相同,无法鉴别,故D选.
故选D.
点评 本题考查物质的鉴别,为高频考点,题目难度不大,注意碳酸钠和碳酸氢钠的性质的异同,学习中注重相关基础知识的积累.

练习册系列答案
相关题目
19.下列物质中所有原子均满足最外层8电子稳定结构的化合物是( )
| A. | PCl5 | B. | P4 | C. | CCl4 | D. | NH3 |
16.已知某条件下,合成氨反应的数据如下:
N2(g)+3H2(g)?2NH3(g)
起始浓度(mol•L-1):1.0 3.0 0.2
2s末浓度(mol•L-1):0.6 1.8 1.0
4s末浓度(mol•L-1):0.4 1.2 1.4
当用氨气浓度的增加来表示该反应的化学反应速率时,下列说法错误的是( )
N2(g)+3H2(g)?2NH3(g)
起始浓度(mol•L-1):1.0 3.0 0.2
2s末浓度(mol•L-1):0.6 1.8 1.0
4s末浓度(mol•L-1):0.4 1.2 1.4
当用氨气浓度的增加来表示该反应的化学反应速率时,下列说法错误的是( )
| A. | 2~4 s内的平均反应速率为0.2 mol•L-1•s-1 | |
| B. | 前4 s内的平均反应速率为0.3 mol•L-1•s-1 | |
| C. | 前2 s内的平均反应速率为0.4 mol•L-1•s-1 | |
| D. | 2 s末的反应速率为0.4 mol•L-1•s-1 |
3.可逆反应2HI(g)?H2(g)+I2(g)在密闭容器中进行,当下列4项中某项不随时间变化时,才能说明反应已达平衡( )
| A. | 容器内压强 | B. | 平均相对分子质量 | ||
| C. | 各组分浓度 | D. | 混合气体的颜色 |
13.下列说法一定正确的是( )
| A. | 其他条件不变时,增大反应的物质的量,反应速率增大,化学平衡发生移动 | |
| B. | 其他条件不变时,升高温度,化学平衡向放热反应的方向移动 | |
| C. | 其他条件不变时,增大压强,化学反应速率增大,化学平衡发生移动 | |
| D. | 其他条件不变时,使用催化剂,化学反应速率改变,化学平衡不移动 |
17.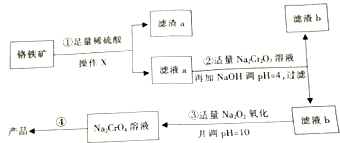 以铬铁矿(主要成分FeO•Cr2O3,含有少量SiO2等)为原料制取铬酸钠晶体(Na2CrO4)工艺流程如图所示.
以铬铁矿(主要成分FeO•Cr2O3,含有少量SiO2等)为原料制取铬酸钠晶体(Na2CrO4)工艺流程如图所示.
已知:①酸性溶液中Cr的+6价易被还原为+3价;当pH>9时Cr以CrO2-形式存在且易被氧化;
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
(1)滤渣a的主要成分的化学式是SiO2;操作X用到的玻璃仪器有烧杯、玻璃棒、和漏斗.
(2)第④步得到产品涉及到的操作有蒸发浓缩、降温结晶、过滤、洗涤等.
(3)第①步反应的离子方程式是FeO+2H+=Fe2++H2O、Cr2O3+6H+=2Cr3++3H2O,第②步产生滤渣b的原因是Fe3+水解生成氢氧化铁沉淀.
(4)已知:1molAl完全燃烧放热a KJ,1mol Fe完全燃烧生成Fe3O4放热b KJ,写出Al与Fe3O4发生铝热反应的热化学方程式8Al(s)+3Fe3O4 (s)=9Fe(s)+4Al2O3 (s),△H=(8a-9b)kJ/mol.
(5)若现有224kg铬铁矿(其中含FeO•Cr2O3 50%),按上述流程最多可以得到Na2CrO4产品的质量是189kg(假设每步均恰好完全转化).
 以铬铁矿(主要成分FeO•Cr2O3,含有少量SiO2等)为原料制取铬酸钠晶体(Na2CrO4)工艺流程如图所示.
以铬铁矿(主要成分FeO•Cr2O3,含有少量SiO2等)为原料制取铬酸钠晶体(Na2CrO4)工艺流程如图所示.已知:①酸性溶液中Cr的+6价易被还原为+3价;当pH>9时Cr以CrO2-形式存在且易被氧化;
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
| 阳离子 | Fe3+ | Fe2+ | Cr3+ |
| 开始沉淀时的pH | 2.7 | 7.6 | |
| 沉淀完全的pH | 3.7 | 9.6 | 9(>9)溶解 |
(2)第④步得到产品涉及到的操作有蒸发浓缩、降温结晶、过滤、洗涤等.
(3)第①步反应的离子方程式是FeO+2H+=Fe2++H2O、Cr2O3+6H+=2Cr3++3H2O,第②步产生滤渣b的原因是Fe3+水解生成氢氧化铁沉淀.
(4)已知:1molAl完全燃烧放热a KJ,1mol Fe完全燃烧生成Fe3O4放热b KJ,写出Al与Fe3O4发生铝热反应的热化学方程式8Al(s)+3Fe3O4 (s)=9Fe(s)+4Al2O3 (s),△H=(8a-9b)kJ/mol.
(5)若现有224kg铬铁矿(其中含FeO•Cr2O3 50%),按上述流程最多可以得到Na2CrO4产品的质量是189kg(假设每步均恰好完全转化).
18.下列物质中,含氢原子数目最多的是( )
| A. | 0.9 mol H2O | B. | 0.3 mol H2SO4 | C. | 0.2 mol NH3 | D. | 0.4 mol CH4 |