题目内容
【题目】电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛. 
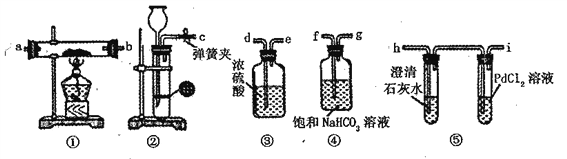
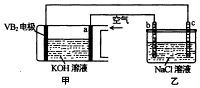
(1)为了减缓海水对钢闸门A和C的腐蚀,图1中,材料B可以选择(填字母序号). a.锌板 b.铜板 c.碳棒
图2中,钢闸门C作极.若用氯化钠溶液模拟海水进行实验,D为石墨块,则D上的电极
反应式为 , 检测该电极反应产物的试剂是 .
(2)微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图3所示(质子交换膜只允许H+自由通过).该电池的正极反应式为 .
(3)电渗析法处理厨房垃圾发酵液,同时得到乳酸(弱酸)的原理如图4所示(图中“HA”表示乳酸 分子,A﹣表示乳酸根离子).
①阳极的电极反应式为 .
②简述浓缩室中得到浓乳酸的原理: .
【答案】
(1)a;阴;2Cl﹣﹣2e﹣═Cl2↑;湿润的淀粉碘化钾试纸放在阳极附近,试纸变蓝,证明生成氯气
(2)O2+4e﹣+4H+═2H2O
(3)4OH﹣﹣4e﹣═2H2O+O2↑;阳极OH﹣放电,c(H+)增大,H+从阳极通过阳离子交换膜进入浓缩室,A﹣通过阴离子交换膜从阴极进入浓缩室,H++A﹣═HA,乳酸浓度增大
【解析】解:(1)形成原电池时,Fe作正极被保护,则要选择活泼性比Fe强的金属作负极,所以选锌;Fe作阴极被保护,则钢闸门C做阴极;电解氯化钠溶液时阳极上氯离子失电子生成氯气,其电极反应为:2Cl﹣﹣2e﹣═Cl2↑,检验氯气用湿润的淀粉碘化钾试纸,即用湿润的淀粉碘化钾试纸放在阳极附近,试纸变蓝,证明生成氯气;所以答案是:a;阴;2Cl﹣﹣2e﹣═Cl2↑;湿润的淀粉碘化钾试纸放在阳极附近,试纸变蓝,证明生成氯气;(2)根据图知,负极上C6H12O6失电子,正极上O2得电子和H+反应生成水,负极的电极反应式为C6H12O6+6H2O﹣24e﹣=6CO2+24H+,正极的电极反应式为O2+4e﹣+4H+═2H2O,所以答案是:O2+4e﹣+4H+═2H2O;(3)①阳极上是阴离子氢氧根离子发生失电子的氧化反应,电极反应式为:4OH﹣﹣4e﹣═2H2O+O2↑,所以答案是:4OH﹣﹣4e﹣═2H2O+O2↑;
②在电解池的阳极上是OH﹣放电,所以c(H+)增大,并且H+从阳极通过阳离子交换膜进入浓缩室;根据电解原理,电解池中的阴离子移向阳极,即A﹣通过阴离子交换膜从阴极进入浓缩室,这样:H++A﹣═HA,乳酸浓度增大,
所以答案是:阳极OH﹣放电,c(H+)增大,H+从阳极通过阳离子交换膜进入浓缩室,A﹣通过阴离子交换膜从阴极进入浓缩室,H++A﹣═HA,乳酸浓度增大.
【考点精析】掌握金属的电化学腐蚀与防护是解答本题的根本,需要知道金属的保护:涂保护层;保持干燥;改变金属的内部结构,使其稳定;牺牲阳极的阴极保护法即用一种更为活泼的金属与要保护的金属构成原电池;外加电源法.

【题目】下表是中学化学教科书中元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答问题.
族 | IA | 0 | |||||||
1 | ① | II A | III A | IV A | V A | VI A | VIIA | ||
2 | ② | ③ | ⑥ | Ne | |||||
3 | ④ | ⑤ | Al | S | |||||
(1)⑥表示的元素是;
(2)②的原子结构示意图是;
(3)由①和③两种元素组成的化合物的化学式是;
(4)④和⑤两种元素的金属性强弱顺序是④⑤(填“<”或“>”).