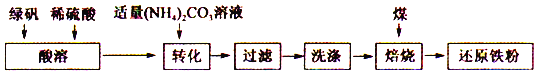
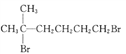题目内容
【题目】下列图示与对应的叙述相符合的是
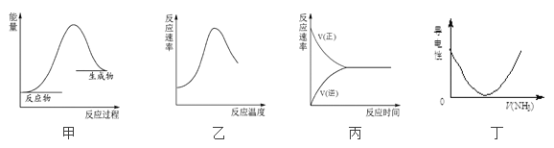
A. 图甲表示燃料燃烧反应的能量变化
B. 图乙表示酶催化反应的反应速率随反应温度的变化
C. 图丙表示可逆反应从加入反应物开始建立化学平衡的过程
D. 图丁表示将NH3通入醋酸溶液的过程中,溶液导电性的变化
【答案】BC
【解析】A.燃料燃烧应放出热量,反应物总能量大于生成物总能量;B.温度过高,酶失去催化活性;C.反应开始时正反应速率大于逆反应速率,平衡时正逆反应速率相等;D.醋酸为弱电解质,反应后生成醋酸铵为强电解质,离子浓度增大导电能力增强,后氨水导电能力减弱。
A.燃料燃烧应放出热量,反应物总能量大于生成物总能量,而题目所给图为吸热反应,选项A错误;B.酶为蛋白质,温度过高,蛋白质变性,则酶催化能力降低,甚至失去催化活性,选项B正确;C.反应开始时正反应速率大于逆反应速率,平衡时正逆反应速率相等,图象符合化学平衡建立特点,选项C正确;D.将NH3通入醋酸溶液的过程中,溶液导电性先增大后减小,图象不符合,选项D错误。答案选BC。

【题目】某温度下,H2(g)+CO2 (g)H2O(g)+CO(g)的平衡常数K= ![]() ,该温度下在甲、乙、丙三个恒容密闭容器中,投入H2 (g)和CO2 (g),其起始浓度如表所示,下列判断不正确的是( )
,该温度下在甲、乙、丙三个恒容密闭容器中,投入H2 (g)和CO2 (g),其起始浓度如表所示,下列判断不正确的是( )
起始浓度 | 甲 | 乙 | 丙 |
c(H2)/molL﹣1 | 0.010 | 0.020 | 0.020 |
c(CO2)/molL﹣1 | 0.010 | 0.010 | 0.020 |
A.平衡时,乙中CO2的转化率大于60%
B.平衡时,甲中和丙中H2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.008 molL﹣1
D.反应开始时,乙中的反应速率最快,甲中的反应速率最慢
【题目】现有部分元素的性质与原子(或分子)结构如下表:
元素编号 | 元素性质与原子(或分子)结构 |
T | 最外层电子数是次外层电子数的3倍 |
X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
Y | M层比K层少1个电子 |
Z | 第3周期元素的简单离子中半径最小 |
(1)元素T在元素周期表中的位置是________。
(2)元素Y与元素Z相比,金属性较强的是______(用元素符号表示),下列表述中能证明这一事实的是______(填序号)。
a.Y单质的熔点比Z单质低 b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈 d.Y最高价氧化物的水化物的碱性比Z强
(3)上述四种元素中有2种元素能形成一种淡黄色的固体,该化合物的电子式是________,所含化学键的类型有________。
(4)元素T和氢元素以原子个数比1∶1化合形成化合物Q,元素X与氢元素形成的化合物W气态时的密度与氧气相等(同温同压),Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式________。