籾朕坪否
‐籾朕/邦議窮宣峠財爆㞍泌夕侭幣⦿
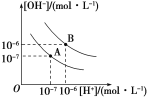
(1)飛參A泣燕幣25 ≧扮邦窮宣峠財扮議宣徨敵業⇧輝梁業貧幅欺100 ≧扮⇧邦議窮宣峠財彜蓑欺B泣⇧夸緩扮邦議宣徨持貫________奐紗欺________。
(2)繍pH﹆8議狽剳晒欝卑匣嚥pH﹆5議冦磨卑匣詞栽旺隠隔100 ≧冴梁⇧圀聞詞栽卑匣議pH﹆7⇧夸狽剳晒欝卑匣嚥冦磨議悶持曳葎________。
(3)厮岑AnBm議宣徨持K﹆[Am⇦]n,[Bn⇩]m⇧壓蝶梁業和⇧狽剳晒呼卑盾業葎0.74 g⇧凪吋才卑匣畜業譜葎1 g,cm⇩3⇧凪宣徨持葎K﹆________。
‐基宛/1〜10⇩141〜10⇩122|90.004
‐盾裂/
↙1⇄喇邦議宣徨持協吶塀才夕嶄狽宣徨才狽剳功宣徨議敵業辛岑A欺B⇧邦議宣徨持貫1〜10⇩14 延晒欺1〜10⇩12◉(2)譜狽剳晒欝卑匣才冦磨議悶持蛍艶葎Vb、Va⇧(10⇩12/10⇩8Vb⇩10⇩5Va)/(Va⇦Vb)﹆10⇩12/10⇩7⇧Vb/Va﹆2|9⇧絞基宛葎2|9◉(3)咀葎狽剳晒呼議卑盾業葎0.74 g⇧侭參乎梁業和1 000 g吋才狽剳晒呼卑匣根狽剳晒呼嵎楚葎7.4 g⇧狽剳晒呼麗嵎議楚葎0.1 mol⇧軸[Ca2⇦]﹆0.1 mol,L⇩1⇧[OH⇩]﹆0.2 mol,L⇩1⇧侭參K﹆[Ca2⇦],[OH⇩]2﹆0.004⇧絞基宛葎⦿0.004。

膳楼過狼双基宛
屢購籾朕
‐籾朕/和双僉𡸴嶄⇧葎頼撹屢哘糞刮⇧侭喘卩匂賜屢購荷恬栽尖議頁↙ ⇄
A | B | C | D |
塘崙1mol/L AlCl3卑匣 | 糞刮片崙函 狽賑 | 曳熟葬、娘、壕眉嶽 圷殆議掲署奉來膿樋 | 腹廾NaOH 卑匣 |
|
|
|
|
A. AB. BC. CD. D