题目内容
【题目】下列情况会对人体健康造成较大危害的是
A.自来水中通入少量Cl2进行消毒杀菌
B.用SO2漂白食品
C.用食醋清洗热水瓶胆内壁附着的水垢(CaCO3)
D.用小苏打(NaHCO3)发酵面团制作馒头
【答案】B
【解析】
A.因Cl2与水反应生成强氧化性的HClO,具有杀菌消毒作用,但自来水中通入少量Cl2进行消毒杀菌时对人体健康不会造成较大的危害,A不符合题意;
B.二氧化硫不能用来漂白食物,二氧化硫的漂白机理是和有色物质发生反应,食物经二氧化硫漂白后就成分就已经发生了改变,残留的二氧化硫使用后进入人体会和人体发生作用造成损伤。本来二氧化硫就对人有毒了,如果有水和氧气的共同作用下就会反应生成硫酸所以有害的,B符合题意;
C.因酸性CH3COOH>H2CO3,故CaCO3与CH3COOH反应:CaCO3+2CH3COOH=(CH3COO)2Ca+H2O+CO2↑,(CH3COO)2Ca易溶于水,因此可以使用食醋清洗热水瓶胆内壁附着的水垢,C不符合题意;
D.NaHCO3不稳定,加热发生分解反应产生CO2气体:2NaHCO3![]() Na2CO3+H2O+CO2↑,气体逸出使蒸出的馒头松软多孔,D不符合题意;
Na2CO3+H2O+CO2↑,气体逸出使蒸出的馒头松软多孔,D不符合题意;
故合理选项是B。

 阅读快车系列答案
阅读快车系列答案【题目】室温下,某一元弱酸HA的电离常数K=1.6×10-6。向20.00mL浓度约为0.1mol·L-1 HA溶液中逐滴加入0.1000mol·L-1的标准NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列有关问题:
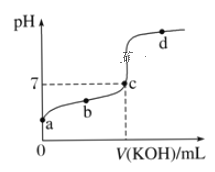
(1)a、b、c、d四点中水的电离程度最大的是_______点,滴定过程中宜选用__________作指示剂,滴定终点在__________(填“c点以上”或“c点以下”)。
(2)滴定过程中部分操作如下,下列各操作使测量结果偏高的是_____(填字母序号)。
A.滴定前碱式滴定管未用标准NaOH溶液润洗
B.用蒸馏水洗净锥形瓶后,立即装入HA溶液后进行滴定
C.滴定过程中,溶液出现变色后,立即停止滴定
D.滴定结束后,仰视液面,读取NaOH溶液体积
(3)若重复三次滴定实验的数据如下表所示,计算滴定所测HA溶液的物质的量浓度为_____mol/L。(保留4位有效数字)
实验序号 | NaOH溶液体积/mL | 待测HA溶液体积/mL |
1 | 21.01 | 20.00 |
2 | 20.99 | 20.00 |
3 | 21.60 | 20.00 |
(4)a点溶液中pH约为________,此时溶液中H2O电离出的c(H+)为________。
