题目内容
下列说法错误的是
| A.仅用KSCN可以检验Fe2+ | B.可以用NaOH溶液检验Fe3+ |
| C.通过化合反应可以得到Fe(OH)3 | D.通过化合反应可以得到FeCl2 |
A
解析试题分析:A、KSCN溶液与氯化亚铁混合没有实验现象,要检验亚铁离子,还需要氧化剂例如氯气等,A不正确;B、氢氧化钠溶液与铁离子反应生成红褐色沉淀氢氧化铁,可以检验铁离子,B正确;C、氢氧化亚铁与氧气、水发生化合反应生成氢氧化铁,C正确;D、氯化铁与铁发生化合反应生成氯化亚铁,D正确,答案选A。
考点:考查铁及其化合物转化、亚铁离子、铁离子的检验

练习册系列答案
相关题目
向NaOH和Na2CO3混合溶液中滴加0.1mol/L稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示。下列判断正确的是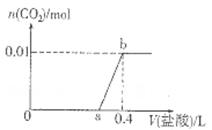
| A.在0-a范围内,只发生中和反应 |
| B.ab段发生反应的离子方程式为:CO32-+2H+=H2O+CO2↑ |
| C.a=0.3 |
| D.原混合溶液中NaOH与Na2CO3的物质的量之比为1:2 |
下列各组物质相互反应能得到Al(OH)3的是
| A.铝与NaOH溶液反应 | B.AlCl3与过量的氨水反应 |
| C.AlCl3与过量的NaOH溶液反应 | D.Al2O3与过量的NaOH溶液反应 |
相同质量的下列物质分别与等浓度的NaOH溶液反应,至体系中均无固体物质,消耗碱量最多的是
| A.Al | B.Al(OH)3 | C.AlCl3 | D.Al2O3 |
若m g Na在足量氯气中燃烧,生成固体的质量为(m+3.55 g),则m g Na与氧气反应,生成固体的质量可能为:①(m+0.8 g) ②(m+1.0 g) ③(m+1.2 g) ④(m+1.6 g) ⑤(m+1.4 g)
| A.①④ | B.①⑤ | C.③④ | D.①②③④⑤ |
下列有关金属铝及其化合物的叙述正确的是
| A.铝在常温下不能与氧气反应 | B.铝不能与氯气反应 |
| C.氧化铝只能与酸反应,不能与碱反应 | D.铝既能溶于酸,又能溶于强碱 |
甲、乙两烧杯中各盛有100mL3mol/L的硫酸和氢氧化钠溶液,向两烧杯中分别加入A克的铝粉,反应结束后测得生成的气体体积为甲:乙=3:4,下列说法正确的是
| A.参加反应的H2SO4为0.2mol | B.参加反应的NaOH约为0.27mol |
| C.加入铝粉的质量A=5.4 | D.与硫酸反应的铝粉的质量7.2g |
已知:2CO(g)+O2(g)=2CO2(g) ΔH= -566 kJ?mol-1
Na2O2(s)+CO2(g) = Na2CO3(s)+1/2O2(g) ΔH= -226 kJ?mol-1
下列表述正确的是(NA代表阿伏伽德罗常数的数值)
| A.1molCO燃烧时放出的热量为283 kJ?mol-1 |
| B.Na2O2(s)+CO(g) = Na2CO3(s)ΔH= -509 kJ?mol-1 |
| C.Na2O2(s)与CO2(g)反应放出226 kJ热量时电子转移数为2NA |
| D.Na2O2和Na2CO3中阴阳离子个数比不同 |
取16.8g碳酸氢钠固体,加热一段时间后,剩余固体的质量为13.7g。把剩余固体加入到100mL 2mol/L的稀硫酸中,充分反应后溶液中H+的浓度约为
| A.3 mol/L | B.2 mol/L | C.1.4 mol/L | D.1 mol/L |