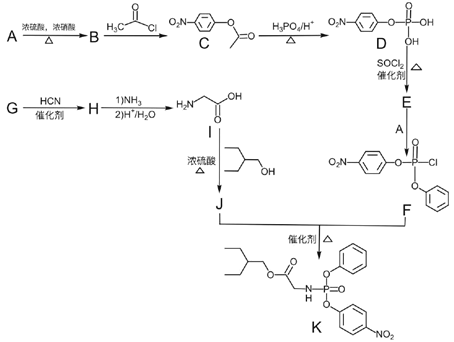
题目内容
【题目】设NA表示阿伏伽德罗常数的值。下列说法正确的是 ( )
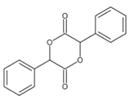
A.0.5 mol 雄黄(As4S4),结构为![]() ,含有NA个 S—S键
,含有NA个 S—S键
B.将 1 mol NH4NO3 溶于适量稀氨水中,所得溶液呈中性,则溶液中 NH4+的数目为 NA
C.107 g Fe(OH)3 分散质的胶体中胶体粒子的数目为NA
D.高温下,16.8 g Fe与足量水蒸气完全反应,转移的电子数为 0.6NA
【答案】B
【解析】
A.图示的雄黄分子中,白球形成了2个共价键、黑球形成了3个共价键,由于硫原子最外层含有6个电子,所以形成了2个共价键,As最外层5个电子,形成3 个共价键,所以白球表示的为S,黑球表示的为As,根据图示,雄黄分子中不存在S-S键,故A错误;
B.将1mol NH4NO3溶于一定浓度的稀氨水中,溶液呈中性,氢离子与氢氧根离子物质的量相等,根据电荷守恒可知,溶液中硝酸根离子与铵根离子的物质的量相等,由于硝酸根离子的物质的量为1mol,则铵根离子的物质的量为1mol,溶液中NH4+的数目为NA,故B正确;
C.107 g Fe(OH)3 的物质的量为![]() =1mol,一个氢氧化铁胶粒是多个氢氧化铁的聚合体,则1mol氢氧化铁所形成的胶粒的个数小于NA个,故C错误;
=1mol,一个氢氧化铁胶粒是多个氢氧化铁的聚合体,则1mol氢氧化铁所形成的胶粒的个数小于NA个,故C错误;
D.16.8g铁的物质的量为0.3mol,而铁和水蒸气反应后变为+![]() 价,故0.3mol铁反应后转移0.8NA个电子,故D错误;
价,故0.3mol铁反应后转移0.8NA个电子,故D错误;
故答案为B。

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
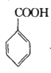
小博士期末闯关100分系列答案【题目】苯甲酰氯(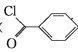 )是制备染料,香料药品和树脂的重要中间体,以光气法制备苯甲酰氯的原理如下(该反应为放热反应):
)是制备染料,香料药品和树脂的重要中间体,以光气法制备苯甲酰氯的原理如下(该反应为放热反应):
 +COCl2
+COCl2![]()
![]() +CO2+HCl
+CO2+HCl
已知物质性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 溶解性 |
苯甲酸 | 122.1 | 249 | 微溶于水,易溶于乙醇、乙醚等有机溶剂 |
碳酰氯(COCl2) | -188 | 8.2 | 较易溶于苯、甲苯等。遇水迅速水解,生成氯化氢,与氨很快反应,主要生成尿素[CO(NH2)2]和氯化铵等无毒物质 |
苯甲酰氯 | -1 | 197 | 溶于乙醚、氯仿和苯。遇水或乙醇逐渐分解,生成苯甲酸或苯甲酸乙酯和氯化氢 |
三氯甲烷(CHCl3) | -63.5 | 63.1 | 不溶于水,溶于醇、苯。极易挥发,稳定性差,450℃以上发生热分解 |
I.制备碳酰氯
反应原理:2 CHCl3+O2![]() 2HCl+COCl2
2HCl+COCl2
甲. 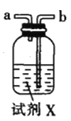 乙.
乙. 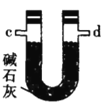 丙.
丙. 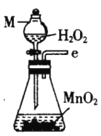 丁.
丁.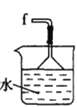 戊.
戊. 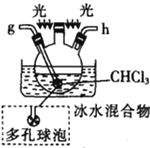
(1)仪器M的名称是____________
(2)按气流由左至右的顺序为___________→c→d→_________→_________→_________→_________→_________.
(3)试剂X是_______________(填名称)。
(4)装置乙中碱石灰的作用是____________。
(5)装置戊中冰水混合物的作用是____________;多孔球泡的作用是________________。
Ⅱ.制备苯甲酰氯(部分夹持装置省略)
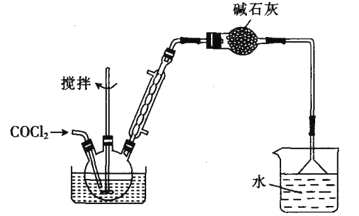
(6)碳酰氯也可以用浓氨水吸收,写出该反应的化学方程式:______________。
若向三颈烧瓶中加入610g苯甲酸,先加热至140~150℃,再通入COCl2,充分反应后,最后产品经减压蒸馏得到562g苯甲酰氯,则苯甲酸的转化率为_________________。