题目内容
【题目】在一定温度下,把2. 0体积的N2和6. 0体积的H2通入一个带活塞的体积可变的容器中,活塞的一端与大气相通,容器中发生如下反应:N2+3H2![]() 2NH3。已知平衡时NH3的浓度是c mol·L-1,现按下列四种配比作为起始物质,分别充入上述容器,并保持温度不变,则达到平衡后,NH3的浓度不为c mol·L-1的是( )
2NH3。已知平衡时NH3的浓度是c mol·L-1,现按下列四种配比作为起始物质,分别充入上述容器,并保持温度不变,则达到平衡后,NH3的浓度不为c mol·L-1的是( )
A. 1.0体积的N2和3.0体积的H2
B. 2.0体积的N2和6.0体积的H2和4.0体积的NH3
C. 4.0体积的NH3和1.0体积的H2
D. 2.0体积的NH3
【答案】C
【解析】试题分析:体系为同温同压下的等效平衡,条件是投料比相等即可。原来的投料比为1:3,A、氮气和氢气的比例为1:3,符合等效平衡的条件,不选A;B、氮气和氢气的比例为1:3,无论氨气的体积多少转化为氮气和氢气的比例都为1:3,所以符合等效平衡,不选B;C、4体积的氨气转化成氮气和氢气后,二者的比例为2:7,不符合等效平衡的要求,选C;D、2体积氨气用极限转化为1体积氮气和3体积氢气,符合等效平衡的条件,不选D。

【题目】某研究小组向某2L密闭容器中加入一定量的固体A和气体B,发生反应A(s)+2B(g)![]() D(g)+E(g)△H=QkJ·mol-1.在T1℃时,反应进行到不同时间测得各物质的物质的量如下表:
D(g)+E(g)△H=QkJ·mol-1.在T1℃时,反应进行到不同时间测得各物质的物质的量如下表:
时间(min) 物质的量(mol) | 0 | 10 | 20 | 30 | 40 | 50 |
B | 2.00 | 1.36 | 1.00 | 1.00 | 1.20 | 1.20 |
D | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
E | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
(1)T1℃时,该反应的平衡常数K=_____;
(2)30min后,只改变某一条件,反应重新达到平衡,根据表中的数据判断改变的条件可能是____(填字母编号).
a.通入一定量的B b.加入一定量的固体A
c.适当缩小容器的体积 d.升高反应体系温度
e.同时加入0.2molB、0.1molD、0.1molE
(3)维持容器的体积和温度T1不变,当向该容器中加入1.60molB、0.20molD、0.20molE和nmolA,达到平衡后,与表格中20分钟时各物质的浓度完全相同时,则投入固体A的物质的量n取值范围_______.
(4)维持容器的体积和温度T1不变,各物质的起始物质的量为:n(A)=1.0mol,n(B)=3.0mol,n(D)=amol,n(E)=0mol,达到平衡后,n(E)=0.50mol,则a=_______.
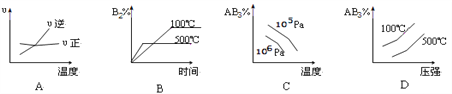
(5)若该密闭容器绝热,实验测得B的转化率B%随时间变化的示意图如图所示由图可知,Q_____0(填“大于”或“小于”),c点v正______v逆(填“大于”、“小于”或“等于”.)