题目内容
【题目】某实验小组学习过氧化钠与水的反应时,向滴有酚酞的水中加入过氧化钠,发现溶液先变红后褪色,对此产生兴趣并进行研究。
(1)写出Na2O2与水反应的化学方程式:______。
(2)甲同学查阅资料:红色褪去的原因是H2O2在碱性条件下氧化了酚酞。
①甲同学通过实验证实了Na2O2与水反应所得溶液中有较多的H2O2:取少量反应所得溶液,加入试剂______(填化学式),有气体产生。
②甲同学利用3% H2O2溶液、酚酞试液、1mol·L-1 NaOH溶液,证实了碱性条件是必需的。
操作 | 现象 | |
实验1 | 向2mL 3%H2O2溶液中加入3滴酚酞试液,振荡,静置5min,再加入5滴1mol·L-1 NaOH溶液 | 观察到______。 |
(3)为了更深入地了解该原理,甲同学继续查阅资料,发现H2O2溶液中相关微粒的物质的量分数X(i)与溶液pH的关系如图所示。
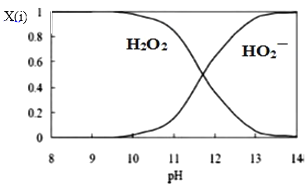
据此,甲同学设计实验2继续研究:
操作 | 现象 | |
实验2 | i.配制20mL 3%H2O2与NaOH的混合溶液,调节pH分别为10~14。 ii.滴入3滴酚酞试液,搅拌后静置,记录酚酞完全褪色的时间 | 得到如图所示实验结果:
|
甲同学由此提出假设I:溶液褪色的主要原因是酚酞被HO![]() 氧化,请结合化学反应速率和化学平衡的相关知识解释此假设:_____。
氧化,请结合化学反应速率和化学平衡的相关知识解释此假设:_____。
(4)乙同学查阅资料,发现酚酞(以H2L表示)在不同pH条件下存在多种结构之间的变化:
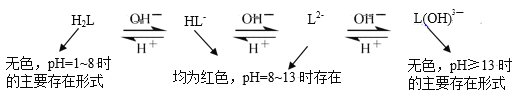
由此提出,甲同学实验2中pH13时红色褪去的原因还存在假设II:_____。
(5)针对假设I、II,小组同学设计了如下实验:
试剂加入顺序 | 现象 | |
实验3 | i.烧杯中加入10mL 2mol·L-1 NaOH溶液、8mL H2O ii.加入3滴酚酞试液 | 溶液变红,然后褪色 |
iii.搅拌、静置后加入2mL 30% H2O2溶液 | _____ | |
iv.向褪色后的溶液中加入盐酸调节pH至12 | 溶液变红,然后褪色 | |
实验4 | i.烧杯中加入10mL 2mol·L-1 NaOH溶液、8mL H2O ii.加入2mL 30% H2O2溶液 iii.搅拌、静置后加入3滴酚酞试液 | 溶液变红,然后褪色 |
iv.向褪色后的溶液中加入盐酸调节pH至12 | 不变红 |
①与L2-和HL-相比较,L(OH)![]() 比前两者更_____被氧化(填“难”或“易”)。
比前两者更_____被氧化(填“难”或“易”)。
②实验3中调节pH至12,溶液变红然后褪色的原因是:_____。
③根据实验得出结论:甲同学实验2中pH13时红色褪去的主要原因是_____(填“假设I”或“假设II”),请依据实验现象阐述理由:_____。
【答案】2Na2O2+2H2O = 4NaOH+O2↑ MnO2 红色褪色 H2O2![]() H+ + HO
H+ + HO![]() ,加入NaOH溶液,消耗电离出的氢离子,平衡正向移动,HO
,加入NaOH溶液,消耗电离出的氢离子,平衡正向移动,HO![]() 浓度增大,酚酞被HO
浓度增大,酚酞被HO![]() 氧化速率增大 溶液褪色的主要原因是酚酞以L(OH)3形式存在 溶液变红,然后褪色 难 酚酞在pH =12时,溶液由于NaOH而呈红色,后来酚酞在pH=12时被HO
氧化速率增大 溶液褪色的主要原因是酚酞以L(OH)3形式存在 溶液变红,然后褪色 难 酚酞在pH =12时,溶液由于NaOH而呈红色,后来酚酞在pH=12时被HO![]() 氧化而褪色 假设I 根据酚酞在不同pH值的存在状态及颜色,排除pH>13酚酞以L(OH)3形式存在而褪色,则说明褪色是由于酚酞被HO
氧化而褪色 假设I 根据酚酞在不同pH值的存在状态及颜色,排除pH>13酚酞以L(OH)3形式存在而褪色,则说明褪色是由于酚酞被HO![]() 氧化而褪色
氧化而褪色
【解析】
Na2O2与水反应生成氢氧化钠和水,反应实质是生成了双氧水,双氧水在二氧化锰催化剂作用下快速反应生成气体;溶液褪色提出假设,并对提出的假设进行用实验来验证。
⑴Na2O2与水反应生成氢氧化钠和水,其化学方程式:2Na2O2+2H2O = 4NaOH+O2↑;故答案为:2Na2O2+2H2O = 4NaOH+O2↑;
⑵①甲同学通过实验证实了Na2O2与水反应所得溶液中有较多的H2O2,利用双氧水在二氧化锰催化剂作用下迅速反应放出大量气泡,因此取少量反应所得溶液,加入试剂MnO2,有气体产生;故答案为:MnO2;
②甲同学利用3% H2O2溶液、酚酞试液、1mol·L-1 NaOH溶液,证实了碱性条件是必需的,实验1在碱性条件下反应,得到的现象为红色褪色;故答案为:红色褪色;
⑶甲同学由此提出假设I:溶液褪色的主要原因是酚酞被HO![]() 氧化,H2O2
氧化,H2O2![]() H++ HO
H++ HO![]() ,加入NaOH溶液,消耗电离出的氢离子,平衡正向移动,HO
,加入NaOH溶液,消耗电离出的氢离子,平衡正向移动,HO![]() 浓度增大,酚酞被HO
浓度增大,酚酞被HO![]() 氧化速率增大;故答案为:H2O2
氧化速率增大;故答案为:H2O2![]() H++ HO
H++ HO![]() ,加入NaOH溶液,消耗电离出的氢离子,平衡正向移动,HO
,加入NaOH溶液,消耗电离出的氢离子,平衡正向移动,HO![]() 浓度增大,酚酞被HO
浓度增大,酚酞被HO![]() 氧化速率增大;
氧化速率增大;
⑷由此提出,甲同学实验2中pH>13时红色褪去的原因还存在假设II:溶液褪色的主要原因是酚酞以L(OH)3形式存在;故答案为:溶液褪色的主要原因是酚酞以L(OH)3形式存在。
⑸根据实验3和实验4对比得出实验3中iii.搅拌、静置后加入2mL 30% H2O2溶液,溶液pH小于13,溶液变为红色,后酚酞被HO![]() 氧化而褪色,因此现象为溶液变红,然后褪色;故答案为:溶液变红,然后褪色;
氧化而褪色,因此现象为溶液变红,然后褪色;故答案为:溶液变红,然后褪色;
①根据实3和实验4分析,实验3中酚酞主要以L2和HL-形式存在,加双氧水,溶液变红,然后褪色,再加盐酸调节pH至12,溶液变红,然后褪色,而实验4盐酸调节pH至12,不变红,说明L(OH)![]() 比前两者更难被氧化;故答案为:难;
比前两者更难被氧化;故答案为:难;
②实验3中调节pH至12,溶液变红然后褪色的原因是:酚酞在pH =12时,溶液由于NaOH而呈红色,后来酚酞在pH=12时被HO![]() 氧化而褪色;故答案为:酚酞在pH =12时,溶液由于NaOH而呈红色,后来酚酞在pH=12时被HO
氧化而褪色;故答案为:酚酞在pH =12时,溶液由于NaOH而呈红色,后来酚酞在pH=12时被HO![]() 氧化而褪色。
氧化而褪色。
③根据实验得出结论:甲同学实验2中pH>13时红色褪去的主要原因是假设I,根据酚酞在不同pH值的存在状态及颜色,排除pH>13酚酞以L(OH)3形式存在而褪色,则说明褪色是由于酚酞被HO![]() 氧化而褪色;故答案为:假设I;根据酚酞在不同pH值的存在状态及颜色,排除pH>13酚酞以L(OH)3形式存在而褪色,则说明褪色是由于酚酞被HO
氧化而褪色;故答案为:假设I;根据酚酞在不同pH值的存在状态及颜色,排除pH>13酚酞以L(OH)3形式存在而褪色,则说明褪色是由于酚酞被HO![]() 氧化而褪色。
氧化而褪色。

【题目】下表中实验操作、现象以及所得出的结论都正确的是![]()
选项 | 实验操作 | 实验现象 | 实验结论 |
A | 向盛有 | 先出现白色沉淀,后出现黄色沉淀 |
|
B | 将适量 | 一支试管出现白色沉淀,另一支试管无明显现象 | 出现的白色沉淀是 |
C | 取少量 | 产生白色沉淀 |
|
D | 湿润的KI淀粉试纸靠近气体Y | 试纸变蓝 | Y可能是 |
A.AB.BC.CD.D
【题目】现有室温下四种溶液,有关叙述不正确的是
编号 | ① | ② | ③ | ④ |
pH | 10 | 10 | 4 | 4 |
溶液 | 氨水 | 氢氧化钠溶液 | 醋酸溶液 | 盐酸 |
A.相同体积③、④溶液分别与 NaOH 完全反应,消耗 NaOH 物质的量:③>④
B.分别加水稀释 10 倍,四种溶液的 pH:①>②>④>③
C.①、④两溶液等体积混合,所得溶液中 c(![]() )>c(Cl-)>c(OH-)>c(H+)
)>c(Cl-)>c(OH-)>c(H+)
D.在③溶液中:c(H+)=c(CH3COO-)+c(CH3COOH)+c(OH-)