��Ŀ����
(1)������A(C4H10O)��һ���л��ܼ���A���Է�����ͼ��ʾ�仯��

��A�����еĹ�����������___________��
��Aֻ��һ��һ��ȡ����B��д����Aת��ΪB�Ļ�ѧ����ʽ________��
��A��ͬ���칹��FҲ�����п�ͼ��A�ĸ��ֱ仯����F��һ��ȡ���������֣�������-OH��ȡ������ F�Ľṹ��ʽ��________��
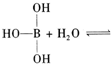
(2)�����HQ��(C6H6O2)��������Ӱ������HQ���������Ȼ�����Һ������ɫ��Ӧ���ҡ�HQ���Ľṹ�Ǹ߶ȶԳƵġ���HQ�����ܷ����ķ�Ӧ�ǣ�ѡ����ţ�___________��
�ټӳɷ�Ӧ ��������Ӧ �ۼӾ۷�Ӧ ��ˮ�ⷴӦ
��HQ����һ����ȡ����ֻ��һ�֡���HQ���Ľṹ��ʽ��__________��
(3)A�롰HQ����һ��������������γ�ˮ��һ��ʳƷ����������TBHQ������TBHQ��������������Һ���� �õ���ѧʽΪC10H12O2Na2�Ļ������TBHQ���Ľṹ��ʽ��___________����ֻд��һ�ּ��ɣ�
��Aֻ��һ��һ��ȡ����B��д����Aת��ΪB�Ļ�ѧ����ʽ________��
��A��ͬ���칹��FҲ�����п�ͼ��A�ĸ��ֱ仯����F��һ��ȡ���������֣�������-OH��ȡ������ F�Ľṹ��ʽ��________��
(2)�����HQ��(C6H6O2)��������Ӱ������HQ���������Ȼ�����Һ������ɫ��Ӧ���ҡ�HQ���Ľṹ�Ǹ߶ȶԳƵġ���HQ�����ܷ����ķ�Ӧ�ǣ�ѡ����ţ�___________��
�ټӳɷ�Ӧ ��������Ӧ �ۼӾ۷�Ӧ ��ˮ�ⷴӦ
��HQ����һ����ȡ����ֻ��һ�֡���HQ���Ľṹ��ʽ��__________��
(3)A�롰HQ����һ��������������γ�ˮ��һ��ʳƷ����������TBHQ������TBHQ��������������Һ���� �õ���ѧʽΪC10H12O2Na2�Ļ������TBHQ���Ľṹ��ʽ��___________����ֻд��һ�ּ��ɣ�
(1)���ǻ�
��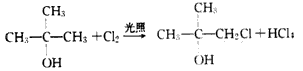
��(CH3)2CHCH2OH
(2)�٢ڣ�
(3)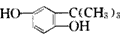 ��
��
��
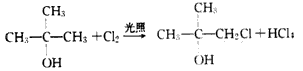
��(CH3)2CHCH2OH
(2)�٢ڣ�

(3)
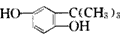 ��
�� 
��ϰ��ϵ�д�
�����Ŀ
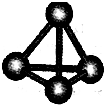 ����A��B��C��D��E��F���ֶ�����Ԫ�أ����ǵ�ԭ��������������D��E���⻯����ӹ��Ͷ���V�ͣ�A��B������������֮����C��������������ȣ�A�ֱܷ���B��C��D�γɵ���������ȵķ��ӣ���A��D���γɵĻ���������¾�ΪҺ̬��
����A��B��C��D��E��F���ֶ�����Ԫ�أ����ǵ�ԭ��������������D��E���⻯����ӹ��Ͷ���V�ͣ�A��B������������֮����C��������������ȣ�A�ֱܷ���B��C��D�γɵ���������ȵķ��ӣ���A��D���γɵĻ���������¾�ΪҺ̬��
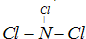
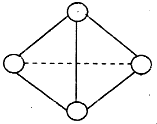 ����A��B��C��D��E��F���ֶ���������Ԫ�أ����ǵ�ԭ��������������D��Eͬ���壬��D���⻯�ﳣ��ʱΪҺ̬��A��B������������֮����C��������������ȣ�A�ֱ���B��C��D�γɵ���������ȵķ��ӣ�
����A��B��C��D��E��F���ֶ���������Ԫ�أ����ǵ�ԭ��������������D��Eͬ���壬��D���⻯�ﳣ��ʱΪҺ̬��A��B������������֮����C��������������ȣ�A�ֱ���B��C��D�γɵ���������ȵķ��ӣ�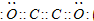
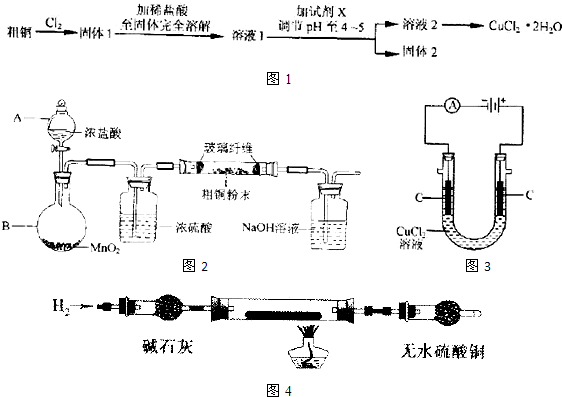
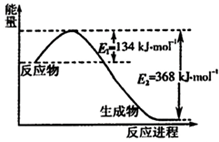 ���ǵ����Ϻ����ḻ��Ԫ�أ������仯������о���������������������Ҫ���壮
���ǵ����Ϻ����ḻ��Ԫ�أ������仯������о���������������������Ҫ���壮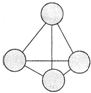 ̼���γɻ���������Ԫ�أ�
̼���γɻ���������Ԫ�أ�