题目内容
【题目】铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下:
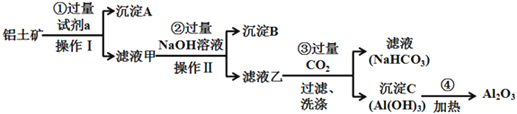
(1)沉淀A的成分是(填化学式)_________。
(2)步骤②中加入过量NaOH溶液发生反应的离子方程式,除了H++OH-=H2O还有:
_____________________________、________________________________;
(3)步骤③中通入过量CO2气体的离子方程式有______________________;
【答案】SiO2 Fe3++3OH-=Fe(OH)3↓ Al3++4OH-=AlO2-+2H2O CO2+OH- = HCO3-;AlO2-+ CO2+2H2O = HCO3- +Al(OH)3 ↓
【解析】
根据工艺流程得出试剂a为盐酸,氧化铝、氧化铁与盐酸反应生成氯化铝和氯化铁,而二氧化硅和盐酸不反应,沉淀A为二氧化硅,滤液中有氯化铝、氯化铁、过量盐酸,再加氢氧化钠溶液,得到氢氧化铁沉淀和偏铝酸钠溶液,过滤,沉淀B为氢氧化铁,滤液为偏铝酸钠与二氧化碳反应生成氢氧化铝和碳酸氢钠溶液,氢氧化铝加热变为氧化铝。
(1)二氧化硅不与盐酸反应,因此沉淀A的成分是(填化学式) SiO2,故答案为:SiO2。
(2)步骤②滤液主要是氯化铝、氯化铁、过量盐酸,加入过量NaOH溶液,先发生酸碱中和反应,再与铁离子和铝离子反应,发生反应的离子方程式,除了H++OH- = H2O还有:Fe3++3OH-=Fe(OH)3↓、Al3++4OH-=AlO2-+2H2O;故答案为:Fe3++3OH-=Fe(OH)3↓、Al3++4OH-=AlO2-+2H2O。
(3)步骤③中通入过量CO2气体,先氢氧化钠和二氧化碳反应,再是偏铝酸钠和二氧化碳反应生成碳酸氢钠和氢氧化铝,其离子方程式有CO2+OH- = HCO3-;AlO2-+ CO2+2H2O = HCO3- +Al(OH)3 ↓,故答案为:CO2+OH- = HCO3-;AlO2-+ CO2+2H2O = HCO3- +Al(OH)3 ↓。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】资料显示“强酸性或强碱性溶液可使品红溶液褪色”。某兴趣小组探究SO2使品红溶液褪色的原因,实验如下。
Ⅰ.探究体现漂白性的主要微粒
实验一:将SO2分别通入0.1%品红水溶液和0.1%品红乙醇溶液中。观察到前者褪色而后者不褪色。
实验二:
| 试管中的液体 | 现象 |
a.0.1mol/L SO2溶液(pH=2) | 溶液逐渐变浅,约90s后完全褪色 | |
b.0.1mol/LNaHSO3溶液(pH=5) | 溶液立即变浅,约15s后完全褪色 | |
c.0.1mol/LNa2SO3溶液(pH=10) | 溶液立即褪色 | |
d.pH=10 NaOH溶液 | 红色溶液不变色 | |
e.pH=2 H2SO4溶液 | 红色溶液不变色 |
(1)SO2水溶液中含![]() 的微粒有___。
的微粒有___。
(2)解释NaHSO3溶液显酸性的原因是___。
(3)实验d的目的是___。
(4)由实验一、二可知:该实验条件下,SO2使品红溶液褪色时起主要作用的微粒是___。
Ⅱ.探究褪色过程的可逆性
甲同学:向a实验后的无色溶液中滴入NaOH溶液至pH=10时,溶液颜色不变。
乙同学:向a实验后的无色溶液中滴入Ba(OH)2溶液至pH=10时,生成白色沉淀,溶液变红。
(5)实验方案合理的是___(选填“甲”或“乙”)。结合离子方程式说明其原因是___。
(6)丙同学利用SO2的还原性设计并完成了下列实验:向a实验后的无色溶液中滴入过量___(填编号),使溶液最终恢复红色。也得出结论:该褪色过程是可逆的。
A.稀硝酸 B.氯水 C.双氧水