题目内容
【题目】过氧化钙(CaO2·8H2O)是一种在水产养殖中广泛使用的供氧剂。
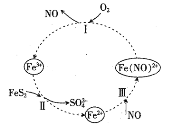
水中溶解氧的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置;加入适量稀H2SO4,待MnO(OH)2与I完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,测定过程中物质的转化关系如下:
![]()
①写出O2将Mn2+氧化成MnO(OH)2的离子方程式:_____________。
②取加过一定量CaO2·8H2O的池塘水样100.00 mL,按上述方法测定水中溶解氧量,消耗0.01000 mol·L1 Na2S2O3标准溶液13.50 mL。计算该水样中的溶解氧(以mg·L1表示),写出计算过程_______。
【答案】O2+2Mn2++4OH-===MnO(OH)2↓ 10.80 mg/L
【解析】
①O2+2Mn2++4OH-===MnO(OH)2↓
②在100.00 mL水样中I2+2S2O32-===2I-+S4O62-
n(I2)=![]() =
=![]() =6.750×10-5 mol
=6.750×10-5 mol
n[MnO(OH)2]= n(I2)= 6.750×10-5 mol
n(O2)=![]() n[MnO(OH)2]=
n[MnO(OH)2]=![]() ×6.750×10-5mol=3.375×10-5 mol
×6.750×10-5mol=3.375×10-5 mol
水中溶解氧=![]() =10.80 mg/L
=10.80 mg/L

练习册系列答案
相关题目