题目内容
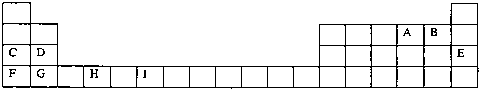
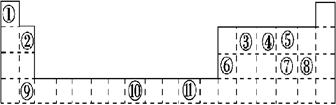
下表为周期表的一部分,表中所列的字母分别代表一种化学元素。

用化学用语回答下列问题:
写出元素f的基态原子核外电子排布式___________________________。
在c6a6分子中,元素c为 杂化,该分子是 分子(填“极性”或“非极性”)。
ci2分子的电子式为_________________________,ci2与ce2比较,沸点较高的是_____________(写分子式)。
第一电离能:h______i;电负性:g______b(填“>”、“<”或“=”)。
下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙正确是 。
A.j位于元素周期表中第四周期、ⅠB族,属于ds区元素
B.d的基态原子中,2p能级为半充满,属于p区元素
C.最外层电子排布式为4s1,一定属于ⅠA族
D.最外层电子排布式为ns2np1,该元素可能是ⅢA族或ⅢB族
将氨水滴入到j的硫酸盐溶液中,先产生蓝色沉淀,然后沉淀逐渐溶解并得到深蓝色溶液,显深蓝色的离子是____________________,写出蓝色沉淀溶解在氨水中的离子方程式______________________________________________________________________。
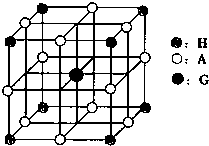
j的金属晶体的晶胞如图所示,则一个晶胞中j原子的个数是_______个。

(1) 1s22s22p5(2分)
(2) sp2 非极性(各1分)
(3) ![]() CS2(各1分)
CS2(各1分)
(4) > <(各1分)
(5) A B(2分)
(6) [Cu(NH3)4]2+(1分) Cu(OH)2+4NH3·H2O=[Cu(NH3)4]2++2OH-+4H2O(3分)
(7) 4(2分)

(13分)下表为周期表的一部分,表中所列的字母分别代表一种化学元素。
|
a |
|
|
|
|
|||||||||||||
|
|
|
|
|
b |
c |
d |
|
|
|||||||||
|
|
|
|
|
|
e |
f |
|
|
|||||||||
|
|
|
|
|
|
g |
|
h |
|
|
|
|
|
|
|
|
|
|
用化学用语回答下列问题:
(1)写出元素g的基态原子核外电子排布式___________________________,
h2+中未成对电子数为 。
(2)在b2a2分子中,元素b为 杂化,该分子是 分子(填“极性”或“非极性”),该分子中σ键和π键的数目比为 。
(3) bd2与bf2比较,沸点较高的是_______(填分子式),原因是 。
(4)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙正确是 。
A.h位于元素周期表中第四周期第VIII族,属于d区元素
B.e的基态原子中,3p能级为半充满,属于p区元素
C.最外层电子排布式为4s2,一定属于IIA族
D.最外层电子排布式为ns2np1,该元素可能是ⅢA族或ⅢB族
(5)科学研究表明,元素b与元素c可以形成一种超硬、耐磨、耐高温的新型无机非金属材料,其化学式为 ,其熔点比金刚石 (填“高”或“低”)。


 其价电子排布式__________。第四周期中电子排布4s轨道上电子数与之相同的还有 元素(填元素符号)。
其价电子排布式__________。第四周期中电子排布4s轨道上电子数与之相同的还有 元素(填元素符号)。