题目内容
2.只有一种试剂可以一次性鉴别(NH4)2SO4、NH4Cl、K2SO4三种溶液,这种试剂是( )| A. | 盐酸 | B. | 氯化钡溶液 | C. | 氢氧化钡溶液 | D. | 氢氧化钠溶液 |
分析 NH4+和OH-反应有刺激性气味的气体生成,SO42-和Ba2+反应生成BaSO4白色沉淀,以此解答该题.
解答 解:三种物质含有的离子有NH4+、Cl-、SO42-,NH4+和OH-反应有刺激性气味的气体生成,SO42-和Ba2+反应生成BaSO4白色沉淀,则可用氢氧化钡溶液检验,现象分别为刺激性气体和白色沉淀、刺激性气体、白色沉淀,可鉴别,
故选C.
点评 本题考查物质的鉴别,此类试题一般要对题目所提供物质的阴、阳离子的鉴别分别分析,然后找出最佳试剂,知道常见阴阳离子的鉴别方法,难度不大.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
12.下列有机物中,一氯代物只有一种的是( )
| A. | 苯 | B. | 甲苯 | C. | 丙烷 | D. | 正丁烷 |
13.下列离子方程式书写正确的是( )
| A. | 铁和稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 实验室用大理石与盐酸反应制取二氧化碳:CO32-+2H+═CO2↑+H2O | |
| C. | 实验室用烧碱溶液吸收氯气:Cl2+2OH-═Cl-+ClO-+H2O | |
| D. | 钠与水的反应:Na+H2O═Na++OH-+H2↑ |
10.已知:2NO2+2NaOH-→NaNO3+NaNO2+H2O;NO+NO2+2NaOH-→2NaNO2+H2O.将224mL(标况下)NO和NO2的混合气体溶于20mL NaOH溶液中,恰好完全反应并无气体逸出,则NaOH溶液的物质的量浓度为( )
| A. | 1 mol/L | B. | 0.5mol/L | C. | 0.25mol/L | D. | 0.2mol/L |
7.氯仿(CHCl3,非电解质)在空气中能发生缓慢氧化,生成剧毒物质光气(COCl2),2CHCl3+O2═2COCl2+2HCl.检验氯仿(CHCl3)是否发生氧化还原反应应选用的试剂是( )
| A. | 水 | B. | NaOH溶液 | ||
| C. | 酚酞 | D. | 硝酸酸化的硝酸银溶液 |
14.如何除去杂质,提纯下列各物质
| 混合物成分 | 提纯所用试剂的化学式 | 离子方程式 |
| (1)MgO中混有少量Al2O3杂质 | NaOH | Al2O3+2OH-=2AlO2-+H2O |
| (2)FeCl2溶液中混少量FeCl3 | Fe | 2Fe3++Fe=3Fe2+ |
| (3)FeCl3溶液中混少量FeCl2 | Cl2 | 2Fe2++Cl2=2Fe3++2Cl- |
| (4)FeSO4溶液中混少量CuSO4 | Fe | Fe+Cu2+=Cu+Fe2+ |
| (5)NaHCO3溶液中混有少量Na2CO3 | CO2 | CO32-+H2O+CO2=2HCO3- |
| (6)Mg溶液中混有少量Si杂质 | NaOH | 2Si+2OH-+H2O=SiO32-+2H2↑ |
| (7)CO2中混有少量HCl杂质 | NaHCO3 | HCO3-+H+=CO2↑+H2O |
| (8)NaCl溶液中混有少量NaBr | Cl2 | Cl2+2Br-=2Cl-+Br2 |
11.以铬酸钾为原料用电化学法制取重铬酸钾的实验装置如图所示,下列说法不正确的是( )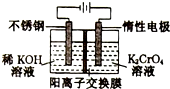

| A. | 电解过程中,K+由阴极室通过阳离子交换膜移阳极室 | |
| B. | 在阴极室,发生的电极反应为:2H++2e-═2H2↑ | |
| C. | 该电解过程实质是电解水 | |
| D. | 在阳极室,通电后溶液逐渐由黄色变为橙色,是因为H+浓度增大,使平衡2CrO42-(黄色)+2H+?Cr2O32-(橙色)+H2O向右移动 |
12.化学与人类的生活密切相关.
(1)铁是人体必需的微量元素,下列物质中加入了铁强化剂的是②(填序号).
①食盐 ②酱油
(2)现有4种食物:①鸡蛋、②,牛肉、③白菜、④胡萝卜.其中,属于碱性食物的是③
④(填序号).
(3)全世界每年因钢铁锈蚀造成大量的损失.某学生欲探究在不同条件下铁锈蚀的快慢,设计了如下实验.
①在一周的观察过程中,他发现实验序号为Ⅰ的试管中铁钉锈蚀速度最慢.
②实验Ⅱ中发生的是电化学腐蚀(填“电化学腐蚀”或“化学腐蚀”).
③下列防止钢铁锈蚀的措施合理的是ac(填字母).
a.自行车的钢圈表面镀镍
b.地下钢铁管道上连接铜块
c.健身器材刷油漆
(4)抗酸药物的作用是中和胃里过多的胃酸.某抗酸药的主要成分是碳酸氢钠,写出碳酸氢钠与盐酸反应的离子方程式:HCO3-+H+=C02↑+H2O.若此抗酸药每片含碳酸氢钠0.42g,取此药一片研碎后与足量的盐酸反应,生成气体在标准状况下的体积为0.12L.
(1)铁是人体必需的微量元素,下列物质中加入了铁强化剂的是②(填序号).
①食盐 ②酱油
(2)现有4种食物:①鸡蛋、②,牛肉、③白菜、④胡萝卜.其中,属于碱性食物的是③
④(填序号).
(3)全世界每年因钢铁锈蚀造成大量的损失.某学生欲探究在不同条件下铁锈蚀的快慢,设计了如下实验.
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 实验 内容 |  | 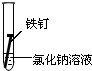 |  |
②实验Ⅱ中发生的是电化学腐蚀(填“电化学腐蚀”或“化学腐蚀”).
③下列防止钢铁锈蚀的措施合理的是ac(填字母).
a.自行车的钢圈表面镀镍
b.地下钢铁管道上连接铜块
c.健身器材刷油漆
(4)抗酸药物的作用是中和胃里过多的胃酸.某抗酸药的主要成分是碳酸氢钠,写出碳酸氢钠与盐酸反应的离子方程式:HCO3-+H+=C02↑+H2O.若此抗酸药每片含碳酸氢钠0.42g,取此药一片研碎后与足量的盐酸反应,生成气体在标准状况下的体积为0.12L.
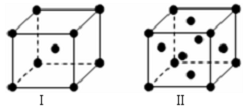 X、Y、Z、M、N、Q、P为元素周期表前四周期的7种元素.其中,X原子核外的M层中只有两对成对电子;Y原子核外的L层电子数是K层的两倍;Z元素原子核外共有3个能级,且最高能级电子数是前两个能级电子数之和;M的内层电子数是最外层电子数的9倍,N的原子序数比M小1,Q在元素周期表的各元素中电负性最大.P元素的第三电子层处于全充满状态,第四电子层只有一个电子.请回答下列问题:
X、Y、Z、M、N、Q、P为元素周期表前四周期的7种元素.其中,X原子核外的M层中只有两对成对电子;Y原子核外的L层电子数是K层的两倍;Z元素原子核外共有3个能级,且最高能级电子数是前两个能级电子数之和;M的内层电子数是最外层电子数的9倍,N的原子序数比M小1,Q在元素周期表的各元素中电负性最大.P元素的第三电子层处于全充满状态,第四电子层只有一个电子.请回答下列问题: