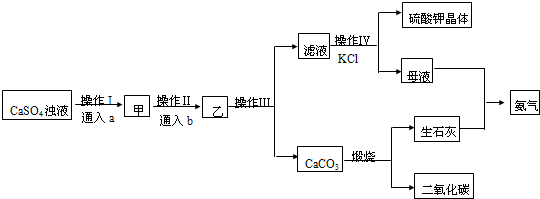
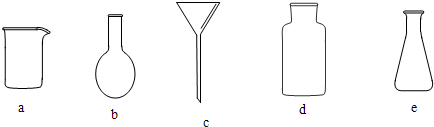
题目内容
18.对于反应2CO+O2=2CO2,在标准状况下,4.48L CO与足量的氧气发生反应,下列有关说法正确的是( )| A. | 生成CO2的物质的量为2 mol | B. | 生成CO2的体积为4.48L | ||
| C. | 生成O2的体积为4.48L | D. | 生成CO2的分子数为1.204×1023个 |
分析 A.根据n=$\frac{V}{{V}_{m}}$计算CO物质的量,再根据方程式计算生成二氧化碳物质的量;
B.体积之比等于化学计量数之比;
C.反应中氧气为反应物,没有氧气生成;
D.根据N=nNA计算CO2的分子数.
解答 解:A.CO物质的量为$\frac{4.48L}{22.4L/mol}$=0.2mol,根据2CO+O2=2CO2,可知生成二氧化碳为0.2mol,故A错误;
B.均为标准状况下,根据2CO+O2=2CO2,可知生成二氧化碳体积为4.48L,故B正确;
C.反应中氧气为反应物,没有氧气生成,故C错误;
D.生成CO2的分子数为0.2mol×6.02×1023mol-1=1.204×1023,故D正确,
故选:BD.
点评 本题考查化学方程式有关计算,比较基础,注意对基础知识的理解掌握.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
8.原子结构模型的演变,经历了五个阶段.其中提出“原子轨道”模型的科学家是( )
| A. | 道尔顿 | B. | 卢瑟福 | C. | 玻尔 | D. | 汤姆生 |
13.设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 18g H2O含有NA个氢原子 | |
| B. | 1.6g氧气含有氧原子的数目为0.1NA | |
| C. | 1mol CO2中含有原子数为NA | |
| D. | 含NA个钠的Na2SO4的物质的量是1mol |
10.实验室需要8.6%的氯化钠溶液100g,某同学用托盘天平称量氯化钠(不到1g的用游码),他把砝码放在左盘,氯化钠放在右盘,当天平平衡时,所称取的氯化钠的实际质量应是( )
| A. | 9.2g | B. | 8.6g | C. | 8g | D. | 7.4g |