题目内容
【题目】化学反应条件是研究化学反应的重要方向。
(1)化工原料异丁烯(C4H8)可由异丁烷(C4H10)直接催化脱氢制备:C4H10(g) ![]() C4H8(g)+H2(g) △H=+139kJ·mol-1
C4H8(g)+H2(g) △H=+139kJ·mol-1
一定条件下,以异丁烷为原料生产异丁烯,在202kPa和808kPa下异丁烷平衡转化率随温度的变化如图所示。
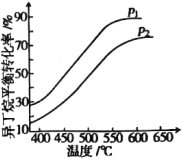
①p1=_______kPa,选择异丁烯制备的温度条件是550~600℃的理由是_________________。
②若平衡混合气中异丁烯的体积分数为25%,则异丁烷的平衡转化率为_______%(保留小数点后1位)。
(2)异丁烷催化脱氢制备异丁烯的研究热点是催化活性组分以及载体的选择。下表是以V-Fe-K-0为催化活性物质,反应时间相同时,测得的不同温度、不同载体条件下的数据。
温度/℃ | 570 | 580 | 590 | 600 | 610 | |
以r-Al2O3为载体 | 异丁烷转化率/% | 36.41 | 36.49 | 38.42 | 39.23 | 42.48 |
异丁烯收率/% | 26. 17 | 27. 11 | 27.51 | 26.56 | 26.22 | |
以TiO2为载体 | 异丁烷转化率/% | 30.23 | 30.87 | 32.23 | 33.63 | 33.92 |
异丁烯收率/% | 25.88 | 27.39 | 28.23 | 28.81 | 29.30 | |
说明:收率=(生产目标产物的原料量/原料的进料量)×100%
①由上表数据,可以得到的结论是____________(填字母序号)。
a 载体会影响催化剂的活性 b 载体会影响催化剂的选择性 c 载体会影响化学平衡常数
②分析以γ-Al2O3为载体时异丁烯收率随温度变化的可能原因:__________。
(3)工业上用复合氧化钴(组成为Co3O4)、碳酸锂以Li/Co(原子比)=1混合,在空气中900℃下加热5小时制备锂离子电池正极材料LiCo O2,写出制备LiCoO2的化学方程式__________。废旧的锂离子电池需要回收,“放电处理”废旧的锂离子电池有利于锂在正极回收的原因是____________。
【答案】202 该反应催化剂活性在550 - 600℃最大,且在此温度下转化率巳经很高,再升高温度转化率提高不大,但消耗能量多 33.3 ab 温度低于590℃,温度升高,催化剂的活性增强,反应速率增大,C4H10(g)![]() C4H8(g)+H2(g)正向移动,异丁烯收率增大,温度高于590℃,催化剂的选择性降低,异丁烯收率减小 4Co3O4+6Li2CO3+O2
C4H8(g)+H2(g)正向移动,异丁烯收率增大,温度高于590℃,催化剂的选择性降低,异丁烯收率减小 4Co3O4+6Li2CO3+O2![]() 12LiCoO2 +6CO2 “放电处理”废旧的锂离子电池有利于锂离子向正极迁移而聚集
12LiCoO2 +6CO2 “放电处理”废旧的锂离子电池有利于锂离子向正极迁移而聚集
【解析】
(1)①异丁烷制备异丁烯的反应是气体分子数增多的反应,增大压强,平衡逆向移动,异丁烷平衡转化率减小,所以P1小于P2,即P1=202kPa。一方面,催化剂需要合适的温度活性才会最好,另一方面,异丁烷制备异丁烯的反应是个吸热反应,温度太低,异丁烷的转化率太低,温度太高,异丁烷的转化率增大程度不大,且会消耗大量的能量。即该反应催化剂活性在550 - 600℃最大,且在此温度下转化率巳经很高,再升高温度转化率提高不大,但消耗能量多,故答案为:202;该反应催化剂活性在550 - 600℃最大,且在此温度下转化率巳经很高,再升高温度转化率提高不大,但消耗能量多;
②设异丁烷起始值为1,变化值为x,则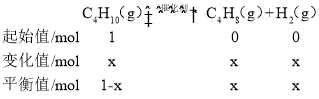 ,25%=
,25%=![]() ,解得x=
,解得x=![]() ,则异丁烷的平衡转化率=
,则异丁烷的平衡转化率=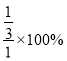 =33.3%,故答案为:33.3%;
=33.3%,故答案为:33.3%;
(2)①a.由表格可知,温度相同时,载体不同,异丁烷转化率不同,故载体会影响催化剂活性,a正确;
b.由表格可知,温度相同时,载体不同,异丁烯的收率不同,故载体会影响催化剂的选择性,b正确;
c.化学平衡常数只和温度有关,温度不变,化学平衡常数不变,c错误;
综上所述,ab正确,故答案为:ab;
②温度低于590℃,温度升高,催化剂的活性增强,反应速率增大,C4H10(g)![]() C4H8(g)+H2(g)正向移动,异丁烯收率增大,温度高于590℃,催化剂的选择性降低,异丁烯收率减小,故答案为:温度低于590℃,温度升高,催化剂的活性增强,反应速率增大,C4H10(g)
C4H8(g)+H2(g)正向移动,异丁烯收率增大,温度高于590℃,催化剂的选择性降低,异丁烯收率减小,故答案为:温度低于590℃,温度升高,催化剂的活性增强,反应速率增大,C4H10(g)![]() C4H8(g)+H2(g)正向移动,异丁烯收率增大,温度高于590℃,催化剂的选择性降低,异丁烯收率减小;
C4H8(g)+H2(g)正向移动,异丁烯收率增大,温度高于590℃,催化剂的选择性降低,异丁烯收率减小;
(3)结合原子守恒、得失电子守恒可得方程式为:4Co3O4+6Li2CO3+O2![]() 12LiCoO2 +6CO2,放电时,阳离子向正极移动,即“放电处理”废旧的锂离子电池有利于锂离子向正极迁移而聚集,故答案为:4Co3O4+6Li2CO3+O2
12LiCoO2 +6CO2,放电时,阳离子向正极移动,即“放电处理”废旧的锂离子电池有利于锂离子向正极迁移而聚集,故答案为:4Co3O4+6Li2CO3+O2![]() 12LiCoO2 +6CO2;“放电处理”废旧的锂离子电池有利于锂离子向正极迁移而聚集。
12LiCoO2 +6CO2;“放电处理”废旧的锂离子电池有利于锂离子向正极迁移而聚集。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案