题目内容
下列说法正确的是( )
| A、自然界中含有大量的游离态的硅,纯净的硅晶体可用于制作计算机芯片 |
| B、硅酸钠的水溶液俗称水玻璃,可用作木材防腐剂 |
| C、水泥、玻璃、水晶都是硅酸盐制品 |
| D、二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
考点:硅和二氧化硅,铜金属及其重要化合物的主要性质
专题:碳族元素
分析:A.硅在自然界以化合态存在;
B.水玻璃为硅酸钠溶液,具有防腐、防火作用;
C.水晶的主要成分为二氧化硅;
D.二氧化硅可与氢氟酸反应.
B.水玻璃为硅酸钠溶液,具有防腐、防火作用;
C.水晶的主要成分为二氧化硅;
D.二氧化硅可与氢氟酸反应.
解答:
解:A.硅为亲氧元素,在自然界以化合态存在,故A错误;
B.水玻璃为硅酸钠溶液,具有防腐、防火作用,故B正确;
C.水晶的主要成分为二氧化硅,水泥、玻璃是硅酸盐制品,故C错误;
D.二氧化硅可与氢氟酸反应,故D错误.
故选B.
B.水玻璃为硅酸钠溶液,具有防腐、防火作用,故B正确;
C.水晶的主要成分为二氧化硅,水泥、玻璃是硅酸盐制品,故C错误;
D.二氧化硅可与氢氟酸反应,故D错误.
故选B.
点评:本题综合考查硅及其化合物的性质以及应用,为高频考点,侧重于元素化合物知识的综合理解和运用的考查,主要相关基础知识的积累,难度不大.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
化学与生活密切相关,下列说法错误的是( )
| A、水是人类不可缺少的营养物质 |
| B、工业废水“再生”处理后可用于城市道路的保洁 |
| C、地沟油的主要成分是高级脂肪酸酯 |
| D、天宫一号中使用的碳纤维是一种新型有机高分子材料 |
常温时,下列各溶液中,离子的物质的量浓度关系正确的是( )
| A、饱和碳酸钠溶液中:c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3) |
| B、pH=2的醋酸中:c(H+)=0.02mol?L-1 |
| C、0.1mol?L-1氯化铵溶液中:c(H+)>c(OH-)>c(Cl-)>c(NH4+) |
| D、pH=12的NaOH溶液与等体积0.01mol?L-1氯化铵溶液混合后所得溶液中:c(Na+)=c(NH4+) |
化合物A、B、C、D各由两种元素组成,甲、乙、丙是短周期元素的三种单质.这些常见的化合物与单质之间存在如下关系(已知C是一种有机物),以下结论不正确的( )

| A、常温下,化合物A、B、C、D均为气体 |
| B、如图所示的五个转化关系中,有三个是化合反应 |
| C、如图所示的五个转化关系中,均为氧化还原反应 |
| D、上述转化关系所涉及的化合物中只有一种是电解质 |
下列对应的表达方式错误的是( )
A、Cl-的结构示意图: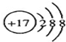 | ||
B、氢氧根离子的电子式: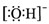 | ||
C、碳-12原子:
| ||
| D、HClO的结构式:H-Cl-O |
下列贮存化学试剂的方法错误的是( )
| A、新制的氯水保存在棕色细口瓶中,并放在阴凉处 |
| B、金属钠保存在煤油中 |
| C、FeSO4溶液存放在加少量铁粉的试剂瓶中 |
| D、烧碱溶液置于带玻璃塞的磨口试剂瓶 |
现有V L 0.5mol/L的盐酸,欲将其浓度扩大一倍,以下方法中最宜采用的是( )
| A、加热浓缩到原来体积的一半 |
| B、加入0.05mol/L的盐酸0.125V L |
| C、加入10mol/L的盐酸0.1V L,再稀释至1.5 V L |
| D、标况下通入11.2L氯化氢气体 |
