题目内容
【题目】有机物G的分子式为C11H12O3,核磁共振氢谱中有5组吸收峰,是制备负性光致抗蚀剂的原料之一,其合成路线如下:

回答下列问题:
(1)E中官能团的名称为__________。
(2)反应③的反应类型为__________。
(3)由C和F生成G的化学方程式为______________________________。
(4)X分子比G少一个CH2原子团,同时满足下列条件的X的结构有__________种。
①能与FeCl3溶液发生显色反应
②能发生银镜反应,且1 mol X可生成4 mol Ag
③核磁共振氢谱中有5组吸收峰
(5)运用自己所学知识,写出A→B的合成路线。_______________
【答案】羟基和氯原子 还原反应 :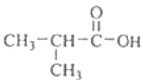 +
+![]()
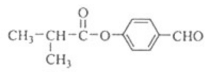
![]() H2O 4 CH2=C(CH3)2
H2O 4 CH2=C(CH3)2![]()
![]()
![]() CH3CCl(CH2Cl)CH3
CH3CCl(CH2Cl)CH3![]() CH3COH(CH2OH)CH3
CH3COH(CH2OH)CH3![]() CH3COH(CHO)CH3
CH3COH(CHO)CH3
【解析】
有机物G的分子式为C11H12O3,核磁共振氢谱中有5组吸收峰,是制备负性光致抗蚀剂的原料之一,所以G的结构简式 ,断酯基为
,断酯基为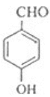 和
和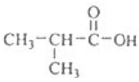 ,所以C的结构简式为
,所以C的结构简式为 ,F的结构简式为
,F的结构简式为![]() ,根据
,根据 逆推E的结构简式为
逆推E的结构简式为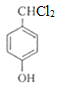 ,以此分析解答本题。
,以此分析解答本题。
(1)由上述可知E的结构简式为 ,所以E中官能团的名称为羟基和氯原子,故答案:羟基和氯原子;
,所以E中官能团的名称为羟基和氯原子,故答案:羟基和氯原子;
(2)由框图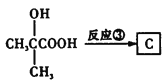 ,且C的结构简式为
,且C的结构简式为 ,所以反应③的反应类型为取代反应,故答案:还原反应;
,所以反应③的反应类型为取代反应,故答案:还原反应;
(3)由C的结构简式为 ,F的结构简式为
,F的结构简式为![]() ,由C和F生成G的化学方程式为:
,由C和F生成G的化学方程式为: +
+![]()

![]() H2O,故答案:
H2O,故答案: +
+![]()
![]()

![]() H2O;
H2O;
(4)由G的结构简式 ,X分子比G少一个CH2原子团,同时满足①能与FeCl3溶液发生显色反应,说明苯环上有羟基,②能发生银镜反应,且1 mol X可生成4 mol Ag,说明含有两个醛基,③核磁共振氢谱中有5组吸收峰的同分异构体由:
,X分子比G少一个CH2原子团,同时满足①能与FeCl3溶液发生显色反应,说明苯环上有羟基,②能发生银镜反应,且1 mol X可生成4 mol Ag,说明含有两个醛基,③核磁共振氢谱中有5组吸收峰的同分异构体由: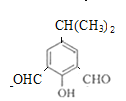 (两个醛基上移,共2种),
(两个醛基上移,共2种),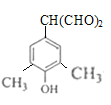 (两个甲基上移共2中),所以共有4种;故答案:4;
(两个甲基上移共2中),所以共有4种;故答案:4;
(5)由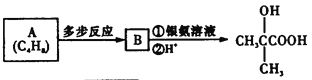 逆推B的结构简式为
逆推B的结构简式为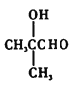 ,A的结构简式为CH2=C(CH3)2,所以A→B的合成路线为:CH2=C(CH3)2
,A的结构简式为CH2=C(CH3)2,所以A→B的合成路线为:CH2=C(CH3)2![]()
![]()
![]() CH3CCl(CH2Cl)CH3
CH3CCl(CH2Cl)CH3![]() CH3COH(CH2OH)CH3
CH3COH(CH2OH)CH3![]() CH3COH(CHO)CH3,所以答案:CH2=C(CH3)2
CH3COH(CHO)CH3,所以答案:CH2=C(CH3)2![]()
![]()
![]() CH3CCl(CH2Cl)CH3
CH3CCl(CH2Cl)CH3![]() CH3COH(CH2OH)CH3
CH3COH(CH2OH)CH3![]() CH3COH(CHO)CH3。
CH3COH(CHO)CH3。

 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案【题目】著名化学家徐光宪在稀土化学等领域取得了卓越成就,被誉为“稀土界的袁隆平”。稀土元素包括钪、钇和镧系元素。请回答下列问题:
(1)写出基态二价钪离子(Sc2+)的核外电子排布式____,其中电子占据的轨道数为 ____。
(2)在用重量法测定镧系元素和使镧系元素分离时,总是使之先转换成草酸盐,然后经过灼烧而得其氧化物,如2LnCl3+3H2C2O4+nH2O=Ln2(C2O4)3nH2O+6HCl。
①H2C2O4中碳原子的杂化轨道类型为____;1 mol H2C2O4分子中含σ键和π键的数目之比为 ___。
②H2O的VSEPR模型为 ___;写出与H2O互为等电子体的一种阴离子的化学式_______。
③HCI和H2O可以形成相对稳定的水合氢离子盐晶体,如HCl2H2O,HCl2H2O中含有H5O2+,结构为![]() ,在该离子中,存在的作用力有___________
,在该离子中,存在的作用力有___________
a.配位键 b.极性键 c.非极性键 d.离子键 e.金属键 f氢键 g.范德华力 h.π键 i.σ键
(3)表中列出了核电荷数为21~25的元素的最高正化合价:
元素名称 | 钪 | 钛 | 钒 | 铬 | 锰 |
元素符号 | Sc | Ti | V | Cr | Mn |
核电荷数 | 21 | 22 | 23 | 24 | 25 |
最高正价 | +3 | +4 | +5 | +6 | +7 |
对比上述五种元素原子的核外电子排布与元素的最高正化合价,你发现的规律是___________
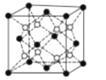
(4)PrO2(二氧化镨)的晶胞结构与CaF2相似,晶胞中Pr(镨)原子位于面心和顶点。假设相距最近的Pr原子与O原子之间的距离为a pm,则该晶体的密度为_____gcm-3(用NA表示阿伏加德罗常数的值,不必计算出结果)。