题目内容
【题目】有 X、Y、Z 三种元素,X 是有机化合物中必含的元素, Y 是地壳里含量最多的元素,Z 是质量最轻的元素。X、Y、Z 三种元素组成的有机物 M 能被酸性高锰酸钾氧化生成 N。为了测定有机物 M 的结构,做如下实验:
①将 4.6 g 有机物 M 完全燃烧,测得生成 0.2mol CO2 和 5.4 g 水;
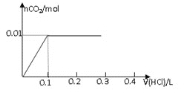
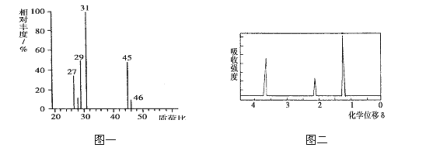
②用质谱仪检测有机物 M,得到如图一所示的质谱图;
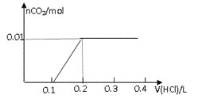
③用核磁共振仪处理有机物 M,得到如图二所示图谱,图中三个峰面积之比为1:2:3
试回答下列问题:
⑴M 的结构简式是______________。
⑵N 中含有的官能团的结构简式为_________________________。
【答案】CH3CH2OH —COOH
【解析】
(1)根据质荷比可以知道,有机物M的相对分子质量;根据n=![]() 计算生成的水的物质的量,计算碳元素、氢元素的质量,根据质量守恒判断有机物M是否含有氧元素,若含有氧元素,计算氧元素质量、氧原子物质的量,根据原子守恒确定有机物M中C、H、O原子个数比值确定最简式,再由核磁共振氢谱可以知道,该有机物分子中有3中化学环境不同的H原子,三种H原子数目之比为1:2:3,结合有机物的分子式确定其可能的结构;
计算生成的水的物质的量,计算碳元素、氢元素的质量,根据质量守恒判断有机物M是否含有氧元素,若含有氧元素,计算氧元素质量、氧原子物质的量,根据原子守恒确定有机物M中C、H、O原子个数比值确定最简式,再由核磁共振氢谱可以知道,该有机物分子中有3中化学环境不同的H原子,三种H原子数目之比为1:2:3,结合有机物的分子式确定其可能的结构;
(2)由M 能被酸性高锰酸钾氧化生成 N推出N的结构,写出其官能团的结构简式。
(1)在M的质谱图中,最大质荷比为46,所以其相对分子质量也是46。
将4.6 g该有机物完全燃烧,生成0.2mol CO2和5.4g水,即0.1mol该有机物,含碳:n(C)=n(CO2)=0.2mol,含有的碳原子的质量为m(C)=0.2 mol×12 gmol-1=2.4g,氢原子的物质的量为:n(H)=![]() ×2=0.6 mol,氢原子的质量为m(H)=0.6 mol×1 gmol-1=0.6g,该有机物中m(O)=4.6 g-2.4 g-0.6 g=1.6 g,氧元素的物质的量为n(O)=
×2=0.6 mol,氢原子的质量为m(H)=0.6 mol×1 gmol-1=0.6g,该有机物中m(O)=4.6 g-2.4 g-0.6 g=1.6 g,氧元素的物质的量为n(O)=![]() =0.1mol,则n(有机物):n(C):n(H):n(O)=0.1mol:0.2mol:0.6 mol:0.1 mol=1:2:6:1,所以M分子式为:C2H6O。
=0.1mol,则n(有机物):n(C):n(H):n(O)=0.1mol:0.2mol:0.6 mol:0.1 mol=1:2:6:1,所以M分子式为:C2H6O。
由核磁共振氢谱可以知道,该有机物分子中有3中化学环境不同的H原子,三种H原子数目之比为1:2:3,故该有机物结构式为CH3CH2OH,
因此,本题正确答案是:CH3CH2OH;
(2)根据以上分析,M为乙醇,由M 能被酸性高锰酸钾氧化生成 N可知,N为乙酸CH3COOH,N 中含有的官能团的结构简式为—COOH,
因此,本题正确答案是:—COOH。

【题目】请按要求回答问题。
(1)Si的基态原子核外电子排布式____,S的基态原子核外有____个未成对电子
(2)用“<”“>”填空
离子半径 | 电负性 | 熔点 | 酸性 |
O2-____Na+ | N___O | 金刚石_____晶体硅 | 硫酸___高氯酸 |
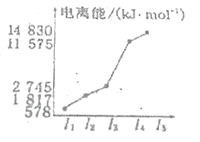
(3)第三周期某元素的电离能情况如图所示,则该元素位于元素周期表第____列
(4)Mn、Fe均为第4周期的过渡元素,两元素的部分电离能数据列于下表:
元素 | Mn | Fe | |
电离能/kJ·mol-1 | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,对此,你的解释是______。
(5)下图能表示HF分子形成的是(____)
a. b.
b.![]()
c. d.
d.