题目内容
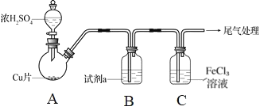
【题目】在3.15晚会中曝光一种劣质净水机的欺骗推销手段:销售人员用如图所示“验水器”检验居民家庭自来水,接通电源后自来水产生大量深色絮状沉淀,而净化后的水再用同一个“验水器”检验,再次接通电源后水没有明显变化依然澄清透明。关于该实验下列分析正确的是( )

A.净化水导电能力理论上比自来水强
B.两次通电可能通过开关反转正负极
C.两次通电的阴极反应产生气体不同
D.金属电极可能采用的是铝或铁材质
【答案】B
【解析】
A. 净化水中离子浓度小于自来水中离子浓度,因此净化水导电能力理论上比自来水弱,故A错误;
B. 根据图中双向开关得出两次通电可能通过开关反转正负极,故B正确;
C. 前后两次通电的阴极反应产生气体都为氢气,阳极反应不相同,故C错误;
D. 接通电源后自来水产生大量深色絮状沉淀,说明金属电极可能采用的是铁材质,故D错误。
综上所述,答案为B。

【题目】下图分离乙酸乙酯、乙醇、乙酸的混合物,可按下列步骤进行分离:
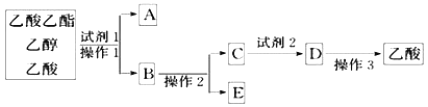
(1)试剂1最好选用_______;
(2)操作1是_______;
(3)试剂2最好选用_______;
(4)操作2是_______;
【题目】某小组在Fe2+检验实验中观察到异常现象,为探究“红色褪去”的原因,进行如下实验:
编号 | 实验I | 实验II | 实验III |
实验步骤 |
| 将实验I褪色后的溶液分三份分别进行实验
| 为进一步探究“红色褪去”的原因,又进行以下实验 ① ②取反应后的溶液,滴加盐酸和BaCl2溶液 |
现象 | 溶液先变红,片刻后红色褪去,有气体生成(经检验为O2) | ①无明显现象 ②溶液变红 ③产生白色沉淀 | ①溶液变红,一段时间后不褪色。 ②无白色沉淀产生 |
分析上述三个实验,下列叙述不正确的是
A.在此实验条件下H2O2氧化Fe2+的速率比氧化SCN-的速率快
B.通过实验Ⅱ推出实验Ⅰ中红色褪去的原因是由于SCN-被氧化
C.通过实验Ⅰ和实验Ⅲ对比推出红色褪去只与H2O2的氧化性有关
D.综上所述,实验Ⅰ中红色褪去的原因与化学平衡移动原理无关