题目内容
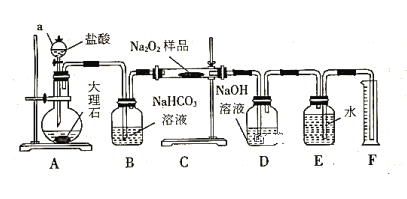
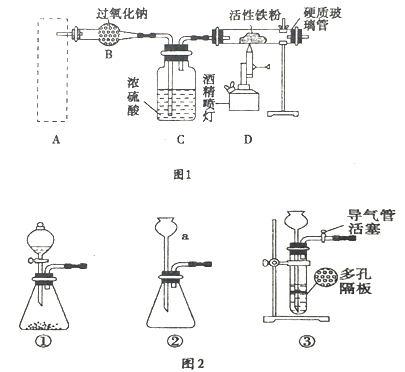
【题目】Fe3O4是重要的化学试剂,铁粉在氧气中燃烧是制取它最为常见和快捷的方法.图1是制取四氧化三铁的系列装置,A装置用于制取二氧化碳气体,并要求气流稳定,流速可控。
请回答下列问题:
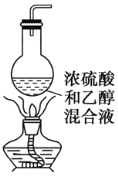
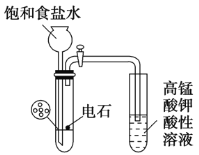
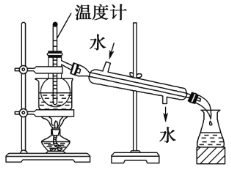
(1)图2中仪器a的名称是___________.
(2)根据题目要求,在图2中最好选择______(填序号)作为A装置.
(3)对图2中装置①进行气密性检查的方法是___________,向分液漏斗中加足量水,过一会儿,水不再下滴,说明装置①的气密性良好.
(4)在B装置中发生主要反应的化学方程式是_________________.
(5)当产生的气体与事先预热的铁粉接触时,在硬质玻璃管中将观察到的明显现象是___________________________________________.
(6)若铁粉被完全消耗,某同学为确定生成物中有+2价铁,取少量生成物于试管中,加入适量的稀硫酸溶解.
①写出溶解过程发生反应的离子方程式_____________________________.
②写出确定+2价铁所用试剂名称、操作步骤、实验现象和结论___________________.
【答案】长颈漏斗 ③ 用止水夹夹紧橡胶管 2Na2O2+2CO2=2Na2CO3+O2 铁粉燃烧,有火星 Fe3O4+8H+=2Fe3++Fe2++4H2O 用小试管取少量高锰酸钾溶液,滴入几滴题述溶液,若紫色变浅,说明有Fe2+存在。
【解析】
(1)根据装置图判断仪器名称;
(2)A装置用于制取CO2,并要求气流稳定,流速可控,选择可以随制随停的装置进行试验;
(3)气密性检查需要先密闭装置,然后改变装置内气压,依据液面变化判断气密性是否良好;
(4)装置A中生成CO2,CO2与B中的过氧化钠反应生成碳酸钠和氧气;
(5)CO2与过氧化钠反应生成生成O2,铁在纯氧中燃烧生成Fe3O4;
(6)①Fe3O4与酸反应生成硫酸铁、硫酸亚铁和水;
②检验+2价铁可用高锰酸钾溶液;
(1)由装置图可知仪器a为长颈漏斗;
(2)A装置用于制取CO2,并要求气流稳定,流速可控,选择可以随制随停的装置,因此最好选择装置③;
(3)检查装置气密性的方法为:用止水夹夹紧橡胶管,向分液漏斗中加足量水,过一会儿,水不再滴落,说明气密性良好;
(4)CO2与B中的过氧化钠反应生成碳酸钠和氧气,反应方程式为:2Na2O2+2CO2=2Na2CO3+O2;
(5)CO2与过氧化钠反应生成生成O2,铁在纯氧中燃烧火星四射;
(6)①Fe3O4与酸反应生成硫酸铁、硫酸亚铁和水,反应的离子方程式为:Fe3O4+8H+=2Fe3++Fe2++4H2O;
②检验+2价铁可用高锰酸钾溶液,向溶液中加入高锰酸钾溶液,若溶液颜色变浅,说明Fe2+存在。

 名校课堂系列答案
名校课堂系列答案