题目内容
(1)
已知:N2(g)+O2(g)=2NO(g);ΔH=+180.5 kJ·mol-14NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g);ΔH=-905 kJ·mol-1
4NO(g)+6H2O(g);ΔH=-905 kJ·mol-1
2H2(g)+O2(g)=2H2O(g):ΔH=-483.6 kJ·mol-1
则N2(g)+3H2(g)![]() 2NH3(g)的
2NH3(g)的
(2)在一定条件下,将2 mol N2与5 mol H2混合于一个10 L的密闭容器中,反应情况如图所示:

①求5 min内的平均反应速率v(NH3)________;
②达到平衡时NH3的体积分数为________.
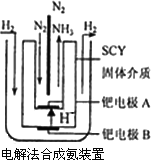
(3)近年来科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多品薄膜做电极,实现了高转化率的电解法合成氨(装置如图).钯电极A上发生的电极反应式是________.
答案:
解析:
解析:
(1)-92.4 kJ·mol-1
(2)①0.04 mol·L-1·min-1
②40%
(3)N2+6e-+6H+![]() 2NH3
2NH3

练习册系列答案
相关题目


 N2(g)+2CO2(g)
N2(g)+2CO2(g) N2(g) +2CO2(g)的△H=___________。
N2(g) +2CO2(g)的△H=___________。

 )
) 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol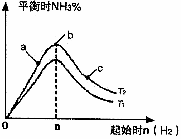


 2NO(g) ΔH
2NO(g) ΔH ,加入相同体积的盐酸时,溶液呈中性,则此盐酸的pH__________
,加入相同体积的盐酸时,溶液呈中性,则此盐酸的pH__________ (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。
 2NO(g) ΔH
2NO(g) ΔH ,加入相同体积的盐酸时,溶液呈中性,则此盐酸的pH__________
,加入相同体积的盐酸时,溶液呈中性,则此盐酸的pH__________ (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。