题目内容
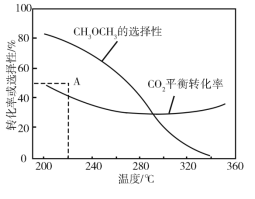
【题目】关于下列各图的叙述,正确的是
A.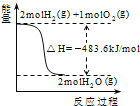 表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241kJ/mol
表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241kJ/mol
B.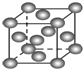 表示Cu形成金属晶体时的堆积方式
表示Cu形成金属晶体时的堆积方式
C.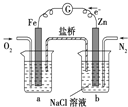 装置中烧杯a中的溶液pH降低
装置中烧杯a中的溶液pH降低
D.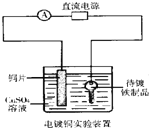 装置中待镀铁制品应与电源正极相连
装置中待镀铁制品应与电源正极相连
【答案】B
【解析】
A、1mol可燃物完全燃烧生成稳定氧化物放出的热量,由图可知焓变是2mol氢气燃烧生成气态水放出的热量,不符合燃烧热概念,A说法错误;
B、图中表示的是面心立方最密堆积属于Cu型,即铜原子形成晶体时采用的堆积方式,B说法正确;
C、烧杯a中通氧气的电极为正极得到电子发生还原反应生成氢氧根离子,溶液pH增大,C说法错误;
D、镀层金属做阳极与电源正极相连,待镀金属做阴极与电源负极相连,D说法错误;
故选B。

练习册系列答案
 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案
相关题目
【题目】以镍废料(主要成分为镍铁合金,含少量铜)为原料,生产NiO的部分工艺流程如下:
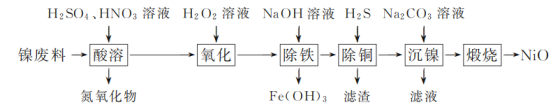
已知:下表列出了几种金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
开始沉淀的pH | 1.5 | 6.5 | 7.7 |
沉淀完全的pH | 3.3 | 9.9 | 9.2 |
(1)“除铁”时需控制溶液的pH范围为________。
(2)“滤渣”的主要成分为________(填化学式)。
(3)“沉镍”时得到碱式碳酸镍[用xNiCO3·yNi(OH)2表示]沉淀。
①在隔绝空气条件下,“煅烧”碱式碳酸镍得到NiO,该反应的化学方程式为________。
②“沉镍”时,溶液pH增大,碱式碳酸镍中Ni元素含量会增加,原因是________。