题目内容
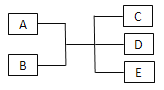
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示。已知Y、W的原子序数之和是Z的3倍,下列说法正确的是

A. 原子半径:X<Y<Z
B. 气态氢化物的稳定性:X>Z
C. 最高价氧化物对应水化物的酸性:Y>W
D. Z、W均可与Mg形成离子化合物
【答案】D
【解析】Y、W的原子序数之和是Z的3倍,设Y的原子序数为x,则Z的原子序数为x+1,W的原子序数为x+10,因此x+x+10=3×(x+1),解得x=7,即Y为N,结合位置关系可知,Z为O,X为Si,W为Cl。A.同周期自左而右原子半径减小,电子层越多原子半径越大,则原子半径为X>Y>Z,A错误;B.非金属性越强,气态氢化物越稳定,则气态氢化物的稳定性为X<Z,B错误;C.Cl的最高价氧化物对应水化物的酸性为含氧酸中酸性最强的酸,非金属性越强最高价含氧酸的酸性越强,故最高价氧化物对应水化物的酸性:W>Y,C错误;D.Z、W可与Mg形成离子化合物氧化镁、氯化镁,D正确;答案选D。

练习册系列答案
相关题目
【题目】(1)选择下列某种答案的序号, 填入下表的空格
①同位素 ②同素异形体 ③同分异构体 ④同系物 ⑤同种物质
物质名称 | 红磷 | 庚烷与 | 氯仿与 | 氕与 | 新戊烷与 | 2-甲基戊烷与 |
相互关系 |
(2)写出下列有机方程式:
①丙烯聚合: ;
②甲苯的硝化反应: ;
③实验室制乙炔: 。