题目内容
【题目】食品防腐剂R的结构简式如图所示:
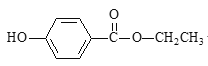
下列说法正确的是
A. R在酸性条件下水解生成乙酸和另一种有机物
B. 1个R分子最多有20个原子共平面
C. 苯环上含2个能与钠反应的官能团和1个乙基的R的同分异构体有10种
D. 1 mol R与3 mol H2反应生成的有机物分子式为C9H18O3
【答案】C
【解析】
A. R在酸性条件下水解生成CH3CH2OH和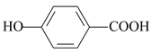 ,无乙酸,A项错误;
,无乙酸,A项错误;
B. -CH2-、-CH3最多分别有1个、2个原子与苯环共平面,R分子最多有18个原子共平面,B项错误;
C. R分子的分子式为C9H10O3,不饱和度=![]() =5,满足条件的同分异构体中,其苯环上应含-OH、-COOH和-CH2CH3,根据“定一移二”方法可判断共有10种同分异构体,C项正确;
=5,满足条件的同分异构体中,其苯环上应含-OH、-COOH和-CH2CH3,根据“定一移二”方法可判断共有10种同分异构体,C项正确;
D. R分子的分子式为C9H10O3,与3 mol H2发生加成反应,分子式为C9H16O3,D项错误;
答案选C。

【题目】蕴藏在海底的大量“可燃冰”,其开发利用是当前解决能源危机的重要课题。CH4(g)+2H2O(g)![]() CO2(g)+4H2(g)ΔH3=+akJ·mol-1
CO2(g)+4H2(g)ΔH3=+akJ·mol-1
化学键 | C—H | H—H | H—O |
键能kJ/mol | b | c | d |
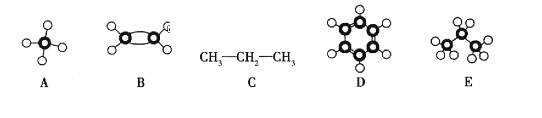
(1)写出甲烷的结构式___________
(2)C=O的键能为_______________kJ/mol(用含a、b、c、d的式子表示)
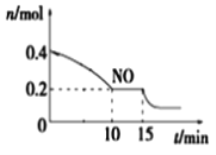
(3)恒温条件下,在体积恒为0.5L的密闭容器中通入一定量甲烷和水蒸气,发生上述反应。测得甲烷物质的量随时间变化如下表所示。0~10min内用H2O的浓度表示该反应的平均速率为υ(H2O)=_____________
时间/min | 0 | 10 | 20 | 40 | 50 | 60 |
n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 | 0.10 |
(4)恒温恒容情况下,下列叙述能说明此反应达到平衡状态的是_______________。
a.混合气体的平均相对分子质量保持不变b.CO2和H2的体积分数比为1﹕4
c.混合气体的密度保持不变d.1molCO2生成的同时有4molH-H键断裂
(5)写出甲烷燃料电池,以KOH溶液为介质时,负极的电极反应式______