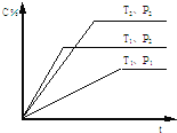
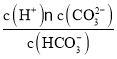题目内容
【题目】下列实验操作及对应解释或结论正确的是![]()
选项 | 实验操作 | 解释或结论 |
A | 向某溶液中滴加盐酸酸化的 | 原溶液中一定含有 |
B | 将 |
|
C | 用蒸馏水润湿的pH试纸测溶液的pH | 一定会使测定结果偏低 |
D | 向混有乙酸和乙醇的乙酸乙酯中加入氢氧化钠溶液 | 除去溶液中的乙酸和乙醇 |
A.AB.BC.CD.D
【答案】B
【解析】
![]() 加入盐酸酸化的氯化钡,可能生成AgCl沉淀,应先加入盐酸,如无现象再加入氯化钡,故A错误;
加入盐酸酸化的氯化钡,可能生成AgCl沉淀,应先加入盐酸,如无现象再加入氯化钡,故A错误;
B.沉淀由白色变为红褐色,可说明氢氧化镁转化为氢氧化铁,可说明![]() 的溶解度小于
的溶解度小于![]() ,故B正确;
,故B正确;
C.如溶液呈中性,则测定结果不变,为防止产生测定误差,因此不能用水湿润pH试纸,故C错误;
D.乙酸乙酯在氢氧化钠溶液中能够发生水解,应用饱和碳酸钠溶液除杂,故D错误;
故答案选B。

练习册系列答案
相关题目
【题目】通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下列实验事实的解释正确的是
现象 | 解释 | |
A | 用洁净的铂丝蘸取某溶液进行焰色反应,火焰呈黄色 | 该溶液中一定含有 |
B |
|
|
C | 某溶液中先加入稀盐酸无现象,再加入氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有 |
D | 铁加入稀硝酸中有气泡产生 | 铁与稀硝酸发生了置换反应 |
A.AB.BC.CD.D