题目内容
4.| 物质 | 分子数 | 质量/g | 物质的量/mol | 摩尔质量/g•mol-1 |
| O2 | 8.0 | |||
| H2SO4 | 3.01×1023 | |||
| H2O | 0.5 |
分析 摩尔质量以g/mol为单位时,各物质的摩尔质量在数值上等于其相对分子量,据此得出各物质的摩尔质量;再结合n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$计算出三者的分子数、质量、物质的量.
解答 解:M(O2)=32g/mol,n(O2)=$\frac{8.0g}{32g/mol}$=0.25mol,N(O2)=0.25×6.02×1023=1.505×1023;
M(H2SO4)=98g/mol,n(H2SO4)=$\frac{3.01×1{0}^{23}}{6.02×1{0}^{23}/mol}$=0.5mol,m(H2SO4)=0.5mol×98g/mol=49g;
M(H2O)=18g/mol,m(H2O)=0.5mol×18g/mol=9g,N(H2O)=0.5×6.02×1023=3.01×1023,
故答案为:
| 物质 | 分子数 | 质量/g | 物质的量/mol | 摩尔质量/g.mol-1 |
| O2 | 1.505×1023 | 0.25 | 32g/mol | |
| H2SO4 | 49 | 0.5 | 98g/mol | |
| H2O | 3.01×1023 | 9 | 18g/mol |
点评 本题考查物质的量的相关计算,题目难度不大,明确物质的量与摩尔质量、阿伏伽德罗常数等物理量之间的关系为解答关键,试题培养了学生的灵活应用能力及化学计算能力.

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
14.已知一定条件下,黄铁矿与硫酸铁溶液反应的化学方程式为FeS2+7Fe2(SO4)3+8H2O═15FeSO4+8H2SO4,下列说法错误的是( )
| A. | FeS2是还原剂,发生氧化反应 | |
| B. | FeSO4是还原产物 | |
| C. | 每生成1molH2SO4,转移14mol电子 | |
| D. | 反应中H2O既不是氧化剂也不是还原剂 |
15.在火星上工作的美国“勇气号”、“机遇号”探测车的一个重要任务就是收集有关Fe2O3及硫酸盐的信息,以证明火星上存在或曾经存在过水,以下叙述正确的是( )
| A. | Fe2O3是一种酸性氧化物 | |
| B. | 检验从火星上带回来的红色物质是否是Fe2O3的操作步骤为:样品-→粉碎-→加水溶解-→过滤-→向滤液中滴加KSCN溶液 | |
| C. | 分别还原a mol Fe2O3所需H2、Al、CO的物质的量之比为 3:2:3 | |
| D. | 明矾属硫酸盐,含结晶水,是混合物 |
19.下列溶液的物质的量浓度是0.5mol/L的是( )
| A. | 20g NaOH溶于1L水中 | |
| B. | 58.5g NaCl溶于水配成1L溶液 | |
| C. | 28g KOH溶于水配成1L溶液 | |
| D. | 通常状况下,11.2L HCl气体溶于水配成1L溶液 |
9.在一个密闭容器中发生如下反应:2SO2(g)+O2(g)?2SO3(g),反应过程中某一时刻测得SO2,O2,SO3的浓度分别为:0.2mol•L-1,0.2mol•L-1,0.2mol•L-1,当反应达到平衡时,可能出现的数据是( )
| A. | c(SO3)=0.4mol•L-1 | B. | c(SO2)=c(SO3)=0.15mol•L-1 | ||
| C. | c(SO2)=0.25mol•L-1 | D. | c(SO2)=c(SO3)=0.4mol•L-1 |
19.下列有关化学用语使用正确的是( )
| A. | C02的电子式::$\underset{\stackrel{…}{O}}{…}$:$\underset{\stackrel{…}{C}}{…}$:$\underset{\stackrel{…}{O}}{…}$ | B. | 中子数为20的氯原子:${\;}_{17}^{20}$Cl | ||
| C. | 乙烯的比例模型 | D. | 铝离子结构示意图: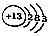 |
20.下列各组顺序的排列不正确的是( )
| A. | 酸性强弱:H2SiO3<H3PO4<H2SO4<HClO4 | |
| B. | 碱性强弱:KOH>NaOH>Mg(OH)2>Al(OH)3 | |
| C. | 熔点:Li<Na<K | |
| D. | 热稳定性:HF>HCl>H2S>PH3 |
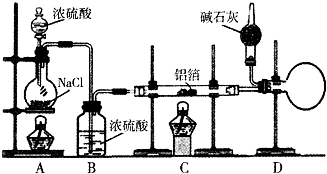 无水氯化铝是有机化工常用的催化剂,氯化铝178℃时升华,极易潮解,遇水发热并产生白色烟雾.氯化铝还易溶于乙醇、氯仿和四氯化碳.实验室可用反应2Al+6HCl(g)$\frac{\underline{\;\;△\;\;}}{\;}$2AlCl3+3H2制备少量无水氯化铝,某同学利用该原理设计如下实验装置:
无水氯化铝是有机化工常用的催化剂,氯化铝178℃时升华,极易潮解,遇水发热并产生白色烟雾.氯化铝还易溶于乙醇、氯仿和四氯化碳.实验室可用反应2Al+6HCl(g)$\frac{\underline{\;\;△\;\;}}{\;}$2AlCl3+3H2制备少量无水氯化铝,某同学利用该原理设计如下实验装置: