题目内容
某强酸性溶液X含有Ba2+、Al3+、N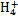 、Fe2+、Fe3+、C
、Fe2+、Fe3+、C 、S
、S 、S
、S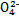 、Cl-、N
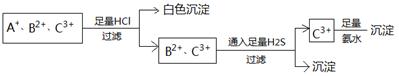
、Cl-、N 中的一种或几种,取该溶液进行实验,实验内容如下:
中的一种或几种,取该溶液进行实验,实验内容如下:

根据以上信息,回答下列问题:
(1)溶液X中除H+外还肯定含有的离子是 ;不能确定是否含有的离子是 ,若要确定其中阳离子的存在,最可靠的化学方法是 。
(2)沉淀G的化学式为 。
(3)写出有关离子方程式:
步骤①中生成A 。
步骤②生成沉淀I 。
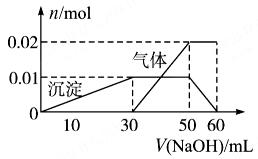
(4)假设测定A、F、I均为0.01 mol,10 mL X溶液中n(H+)="0.04" mol,而沉淀C物质的量0.07 mol,能说明(1)中不能确定的阴离子存在的理由是 。
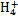 、Fe2+、Fe3+、C
、Fe2+、Fe3+、C 、S
、S 、S
、S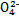 、Cl-、N
、Cl-、N 中的一种或几种,取该溶液进行实验,实验内容如下:
中的一种或几种,取该溶液进行实验,实验内容如下:
根据以上信息,回答下列问题:
(1)溶液X中除H+外还肯定含有的离子是 ;不能确定是否含有的离子是 ,若要确定其中阳离子的存在,最可靠的化学方法是 。
(2)沉淀G的化学式为 。
(3)写出有关离子方程式:
步骤①中生成A 。
步骤②生成沉淀I 。
(4)假设测定A、F、I均为0.01 mol,10 mL X溶液中n(H+)="0.04" mol,而沉淀C物质的量0.07 mol,能说明(1)中不能确定的阴离子存在的理由是 。
(1)Al3+、N 、Fe2+、S
、Fe2+、S Cl-、Fe3+ 取少量X溶液放入试管中,加入几滴KSCN溶液,溶液不变红色说明无Fe3+,若变红则说明含Fe3+(没有取样、取量扣分)
Cl-、Fe3+ 取少量X溶液放入试管中,加入几滴KSCN溶液,溶液不变红色说明无Fe3+,若变红则说明含Fe3+(没有取样、取量扣分)
(2)Fe(OH)3
(3)3Fe2++N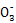 +4H+
+4H+ 3Fe3++NO↑+2H2O Al
3Fe3++NO↑+2H2O Al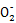 +CO2+2H2O
+CO2+2H2O Al(OH)3↓+HC
Al(OH)3↓+HC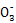
(4)若检验Fe3+肯定存在时,就有Cl-存在,因为肯定存在的离子电荷总数已相等
 、Fe2+、S
、Fe2+、S Cl-、Fe3+ 取少量X溶液放入试管中,加入几滴KSCN溶液,溶液不变红色说明无Fe3+,若变红则说明含Fe3+(没有取样、取量扣分)
Cl-、Fe3+ 取少量X溶液放入试管中,加入几滴KSCN溶液,溶液不变红色说明无Fe3+,若变红则说明含Fe3+(没有取样、取量扣分)(2)Fe(OH)3
(3)3Fe2++N
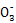 +4H+
+4H+ 3Fe3++NO↑+2H2O Al
3Fe3++NO↑+2H2O Al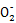 +CO2+2H2O
+CO2+2H2O Al(OH)3↓+HC
Al(OH)3↓+HC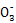
(4)若检验Fe3+肯定存在时,就有Cl-存在,因为肯定存在的离子电荷总数已相等
强酸性溶液X一定不含C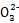 、S
、S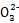 ;在酸性溶液中与Ba(NO3)2溶液混合有沉淀C生成,可知X中含有S
;在酸性溶液中与Ba(NO3)2溶液混合有沉淀C生成,可知X中含有S ,一定无Ba2+;生成气体A只能为NO,所以X中含有还原性物质Fe2+,无N
,一定无Ba2+;生成气体A只能为NO,所以X中含有还原性物质Fe2+,无N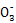 ;溶液B中含有 Fe3+,沉淀G为Fe(OH)3;由气体F可知X中含有N
;溶液B中含有 Fe3+,沉淀G为Fe(OH)3;由气体F可知X中含有N ,由步骤②可知X中含有Al3+;(4)n(NO)="0.01" mol、n(NH3)="0.01" mol、n[Al(OH)3]="0.01" mol、n(H+)="0.04" mol、n(BaSO4)="0.07" mol,依据原子及化合价守恒可知溶液中含有:n(Fe2+)="3n(NO)=0.03" mol、n(N
,由步骤②可知X中含有Al3+;(4)n(NO)="0.01" mol、n(NH3)="0.01" mol、n[Al(OH)3]="0.01" mol、n(H+)="0.04" mol、n(BaSO4)="0.07" mol,依据原子及化合价守恒可知溶液中含有:n(Fe2+)="3n(NO)=0.03" mol、n(N )="0.01" mol、n(Al3+)="0.01" mol、n(H+)="0.04" mol、n(S
)="0.01" mol、n(Al3+)="0.01" mol、n(H+)="0.04" mol、n(S )="0.07" mol,依据电荷守恒2n(Fe2+)+n(N
)="0.07" mol,依据电荷守恒2n(Fe2+)+n(N )+3n(Al3+)+n(H+)="0.14" mol=2n(S
)+3n(Al3+)+n(H+)="0.14" mol=2n(S )
)
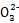 、S
、S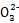 ;在酸性溶液中与Ba(NO3)2溶液混合有沉淀C生成,可知X中含有S
;在酸性溶液中与Ba(NO3)2溶液混合有沉淀C生成,可知X中含有S ,一定无Ba2+;生成气体A只能为NO,所以X中含有还原性物质Fe2+,无N
,一定无Ba2+;生成气体A只能为NO,所以X中含有还原性物质Fe2+,无N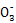 ;溶液B中含有 Fe3+,沉淀G为Fe(OH)3;由气体F可知X中含有N
;溶液B中含有 Fe3+,沉淀G为Fe(OH)3;由气体F可知X中含有N ,由步骤②可知X中含有Al3+;(4)n(NO)="0.01" mol、n(NH3)="0.01" mol、n[Al(OH)3]="0.01" mol、n(H+)="0.04" mol、n(BaSO4)="0.07" mol,依据原子及化合价守恒可知溶液中含有:n(Fe2+)="3n(NO)=0.03" mol、n(N
,由步骤②可知X中含有Al3+;(4)n(NO)="0.01" mol、n(NH3)="0.01" mol、n[Al(OH)3]="0.01" mol、n(H+)="0.04" mol、n(BaSO4)="0.07" mol,依据原子及化合价守恒可知溶液中含有:n(Fe2+)="3n(NO)=0.03" mol、n(N )="0.01" mol、n(Al3+)="0.01" mol、n(H+)="0.04" mol、n(S
)="0.01" mol、n(Al3+)="0.01" mol、n(H+)="0.04" mol、n(S )="0.07" mol,依据电荷守恒2n(Fe2+)+n(N
)="0.07" mol,依据电荷守恒2n(Fe2+)+n(N )+3n(Al3+)+n(H+)="0.14" mol=2n(S
)+3n(Al3+)+n(H+)="0.14" mol=2n(S )
)
练习册系列答案
相关题目
 2NaAlO2+H2O
2NaAlO2+H2O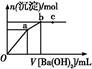
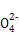 +Ba2+
+Ba2+ BaSO4↓
BaSO4↓