题目内容
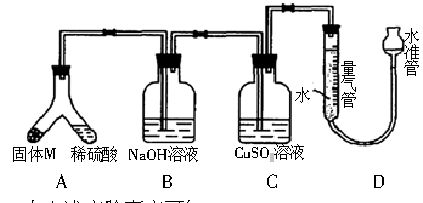
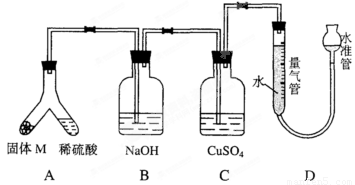
某课外兴趣小组为了探究铁与硫在隔绝空气的条件下反应所得固体M的成分,设计了如下图装置。
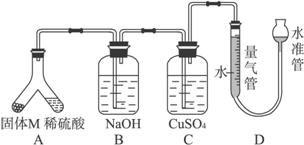
倾斜A使稀硫酸(足量)与固体M充分反应,待反应停止后,B装置增重,C装置中溶液无变化。反应后进入量气管气体的体积为V mL(已折算成标准状况)。
由上述实验事实可知:
(1)①固体M中一定有的物质是__________(填化学式)。理由是_______________________。
②其中一种物质的质量可以确定为____________g(用代数式表示)。
(2)B装置的名称是________________________。
写出B装置中反应的离子方程式___________________________________________________。
(3)C装置的作用是_________________________,如果实验中没有B装置,则C装置中产生的现象是________________________________________。
(4)稀硫酸和固体M反应后溶液中还残留淡黄色固体,该固体是_____________,要分离出该固体,在实验操作中,除烧杯外还需要用到的玻璃仪器是_________________________。
(5)通过进一步实验,测得固体M中各种成分的质量之和小于反应前铁粉和硫粉的质量之和,产生这种现象的原因可能是___________。
a.M中有未反应的铁和硫
b.测定气体体积时水准管的水面高于量气管的水面
c.A中留有反应生成的气体
d.气体进入D装置前未用浓硫酸干燥
(1)①FeS Fe B装置增重、量气管有气体
②![]()
(2)洗气瓶
2OH-+H2S![]() 2H2O+S2-
2H2O+S2-
(3)证明H2S已被完全吸收
黑色沉淀
(4)硫 漏斗、玻璃棒 (5)b、c
解析:(1)产生的气体中有不能被NaOH吸收的气体,证明该气体是H2,则可推断出,Fe与硫隔绝空气条件下反应后的固体M中有过量的Fe,则固体M中一定有FeS、Fe,由生成H2的体积可计算出Fe的质量。
(2)(3)B装置是洗气瓶,用来吸收H2S,C装置用来检验H2S是否吸收干净;若H2S没有吸收干净,则能与CuSO4溶液作用生成黑色的CuS沉淀。
(4)稀硫酸与M反应后还剩余的淡黄色固体为S,要分离出S,需用过滤装置。
(5)测得M中各成分的质量和小于反应前的Fe和S的质量,造成误差的原因可能是计算时A中的气体没有完全进入B或D中,或者是读D中气体体积时水准管的水面高于量气管的水面,造成D中的气体体积是大于1.0×105 Pa时的气体体积。