题目内容
【题目】A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中,A、C及B、D分别是同主族元素;A元素的原子半径是所有主族元素中原子半径最小的;B、D两元素的原子核中质子数之和是A、C两元素原子核中质子数之和的2倍;四种元素所形成的单质中常温下A、B单质是气体,C、D单质是固体。
(1)写出四种元素的名称:A___________B____________C___________D___________。
(2)用电子式表示A2B的形成过程: _________________________。
(3)由B、C两元素所形成的原子个数比为1:1的化合物属于__________(填“离子”或“共价”)化合物,写出它与水反应的离子方程式______________________。
(4)实验室常用A、B两元素所形成的原子个数为1:1的化合物来制备一种常见气体,其化学方程式为_____________。
(5)A2B和A2D的沸点较高者为______________(填化学式)。
【答案】氢 氧 钠 硫 ![]() 离子 2Na2O2+2H2O=4Na++4OH-+O2↑ 2H2O2
离子 2Na2O2+2H2O=4Na++4OH-+O2↑ 2H2O2 ![]() 2H2O+O2↑ H2O
2H2O+O2↑ H2O
【解析】
A、B、C、D是四种短周期元素,它们的原子序数依次增大,A元素的原子半径是所有主族元素中原子半径最小,则A为氢元素;A、C及B、D分别是同主族元素,B、D两元素的原子核中质子数之和是A、C两元素原子核中质子数之和的2倍,则B、D在二、三周期,故C处于第三周期,则C为钠元素;B、D分别是同主族元素,B、D两元素的原子核中质子数之和为2(1+11)=24,故B为氧元素,D为硫元素;其中四种元素所形成的单质中A、B单质是气体,C、D单质是固体,符合题意.
根据以上A为氢元素,B为氧元素,C为钠元素,D为硫元素
(1)四种元素的名称:A 、氢 B、 氧 C、钠 D、 硫。故答案为:A 、氢 B、 氧 C、钠 D、 硫。
(2)水分子是共价化合物,氧原子与氢原子形成两个共用电子对,用电子式表示H2O的形成过程:![]() 。故答案为:
。故答案为:![]() ;
;
(3)B为氧元素,C为钠元素,由两元素所形成的原子个数比为1:1的化合物为Na2O2,由钠离子与过氧根离子构成,属于离子化合物,钠离子与过氧根离子之间为离子键,过氧根离子中氧原子之间为非极性键;过氧化钠与水反应生成氢氧化钠与氧气,反应离子方程式为2Na2O2+2H2O=4Na++4OH-+O2↑,
故答案为:离子;2Na2O2+2H2O=4Na++4OH-+O2↑;
(4)A为氢元素,B为氧元素,两元素所形成的原子个数为1:1的化合物为H2O2,实验室常用H2O2气体O2,反应方程式为2H2O2![]() 2H2O+O2↑ ,故答案为:2H2O2
2H2O+O2↑ ,故答案为:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(5)水分子间形成氢键,H2O和H2S的沸点较高者为H2O。故答案为:H2O。

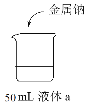
【题目】研究金属钠的性质,实验如下:
实验装置 | 实验方案 | |
液体a | 现象 | |
| 蒸馏水 | I.钠浮在水面,剧烈反应,有少量白雾 |
0.1 mol·L-1盐酸 | II.钠浮在液面,反应比Ⅰ剧烈,有白雾产生 | |
浓盐酸 | III.钠浮在液面,反应比Ⅰ缓慢,产生大量白雾,烧杯底部有白色固体 | |
下列说法不正确的是
A.II中反应的离子方程式为2Na + 2H+ === 2Na+ + H2↑
B.对比I、II、III可知,随着c(H+) 增大,反应的剧烈程度增大
C.实验I、II、III均有白雾产生,说明Na与水或酸反应均放出大量热
D.推测III中浓盐酸的c(Cl-)以及生成的NaCl固体对反应剧烈程度有影响
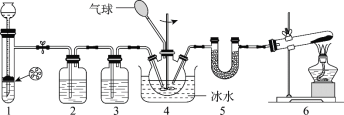
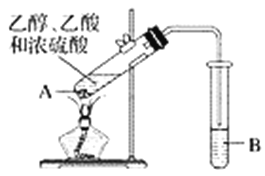
【题目】乙烯是一种重要的基本化工原料,实验小组同学欲制备乙烯并验证其与溴单质的反应类型为加成反应。
I.乙烯的制备
欲利用下图所给装置制备乙烯。反应原理为:CH3CH2OH ![]() CH2=CH2↑+H2O,反应过程中观察到蒸馏烧瓶中溶液逐渐变黑。
CH2=CH2↑+H2O,反应过程中观察到蒸馏烧瓶中溶液逐渐变黑。
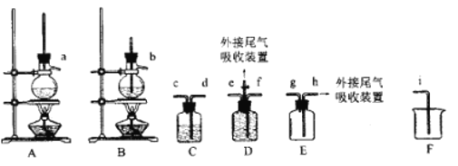
(1)欲收集一瓶乙烯,选择上图中的装置,其连接顺序为_____(按气流方向,用小写字母表示)。
(2)C中盛放的试剂为______,其作用为_____。
(3)在烧杯中混合浓硫酸和乙醇时,应先添加___;实验开始一段时间后发现忘记加碎瓷片,此时应该进行的操作为____。
(4)尾气吸收可采用________(填选项字母)。
A.KMnO4酸性溶液 B.浓硫酸 C.饱和Na2CO3溶液 D.NaOH溶液
II.验证乙烯与溴单质的反应类型为加成反应。
实验小组同学将I中制得的乙烯干燥后,按下列两种方案进行实验。
方案 | 操作 | 现象 |
一 | 将纯净的乙烯通入溴水中 | 溴水褪色 |
二 | 向充满纯净乙烯的塑料瓶中注入适量溴的CC14溶液,振荡 | ①溴的CCl4溶液褪色 ② |
(5)乙烯与溴单质发生加成反应的化学方程式为_________。
(6)方案一不能证明乙烯与溴单质发生了加成反应,原因为_________。
(7)方案二中现象②应为______,要想用此方案证明乙烯与溴单质发生的反应是加成反应,还需补充的实验为:继续向方案二塑料瓶中加入少量______,振荡后,若_____,证明发生了加成反应。